有価証券報告書-第48期(令和2年4月1日-令和3年3月31日)
事業内容
(1) 事業の内容について
当社グループの企業集団は、当社、連結子会社22社及び関連会社3社の合計26社で構成されております。事業の内容は、1.製薬企業等から前臨床試験(注1)、臨床試験(治験)(注2)(注3)及び新薬承認申請業務を受託し、医薬品開発支援を行うCRO(Contract Research Organization)事業、2.当社が独自に開発した経鼻投与製剤(注4)並びに大学やバイオベンチャーの基礎的な知見や技術を育成してビジネス化していくトランスレーショナル リサーチ(TR)事業、3.メディポリス指宿において地熱発電や宿泊施設運営などを行うメディポリス事業を行っております。
具体的には、CRO事業では、安全性研究所において前臨床試験を、薬物代謝分析センターにおいて前臨床試験及び臨床試験の試料分析を、株式会社新日本科学PPDにおいて臨床試験をそれぞれ受託しております。TR事業としては、薬物の鼻粘膜吸収性を高める独自の経鼻投与基盤技術やデバイス、及び薬物の脳移行性を高める独自の送達技術を研究開発し、これらを応用した創薬を行っております。当事業部よりスピンアウトした経鼻片頭痛治療薬の開発会社である米国Satsuma Pharmaceuticals, Inc.、及び経鼻神経変性疾患レスキュー薬の開発会社である国内株式会社SNLDを支援しています。その他、核酸医薬品の開発を行う米国WAVE Life Sciences Ltd.は当事業部を起源としております。メディポリス事業では、環境に配慮した完全閉鎖式バイナリ―地熱発電事業並びに一般社団法人メディポリス医学研究所メディポリス国際陽子線治療センターと連携して、宿泊施設別邸天降る丘と指宿ベイヒルズHOTEL&SPAを運営しています。
香港の新日本科学(亜州)有限公司は、アジアにおける事業を統括し、中国本土の肇慶創薬生物科技有限公司、カンボジア王国のTIAN HU(CAMBODIA)ANIMAL BREEDING RESEARCH CENTER Ltd.では、実験動物の繁殖育成と検疫輸出を行っています。
(注1)前臨床試験:臨床試験に着手する前に、実験動物や細胞・細菌を用いて医薬品等の化学物質の有効性と安全性を確認する試験です。
(注2)臨床試験:ヒトに対する薬の有効性と安全性を確認するために、医療機関で実施する試験です。
(注3)治験:臨床試験のうち、厚生労働省から新薬の承認を得るために実施する試験です。
(注4)経鼻投与製剤:既に市販されている薬剤の剤型に工夫を施し、鼻から投与し、鼻粘膜から吸収させ、治療するシステムのことであります。
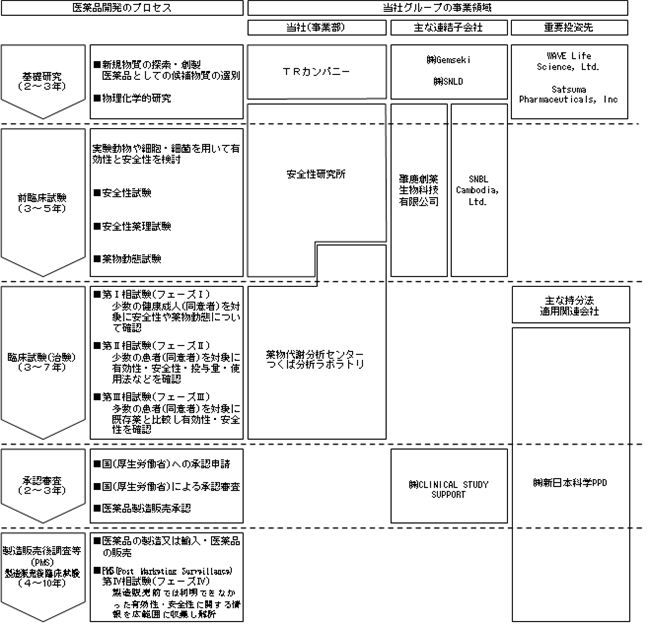
(2) 医薬品開発のプロセスにおける当社グループの事業領域について
製薬企業は、医薬品を開発し、最終的に販売するまでには薬機法に基づく様々な試験を実施し、有効性と安全性を確認します。厚生労働省に新薬承認申請を行うに際しては、それらの試験の成績を添付し、同省諮問機関の専門家による厳密な審査を経て承認が得られるシステムになっております。
医薬品開発のプロセスにおける当社グループの事業領域については、次のとおりであります。
 (3) セグメントについて
(3) セグメントについて
セグメントは、当社と連結子会社22社、持分法適用関連会社3社により、次のとおりCRO事業(前臨床事業・臨床事業)・トランスレーショナル リサーチ事業・メディポリス事業及びその他事業に区分されております。
(注)持分法適用関連会社であります。
当社及び連結子会社のセグメント系統図並びに会社別事業内容は、次のとおりであります。
<セグメント系統図>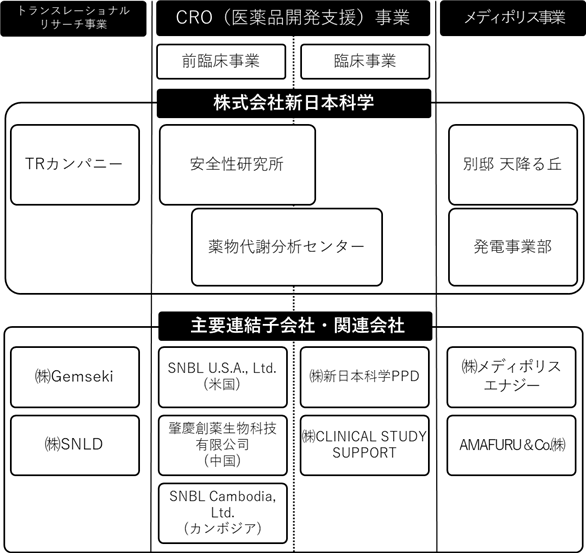 <会社別事業内容>
<会社別事業内容>
(4) 前臨床事業について
前臨床試験とは、製薬企業等により開発された被験物質(注1)の有効性と安全性について、実験動物や細胞・細菌などを用いて調べる試験です。実験動物を用いる前臨床試験は、その後に続く、ヒトによる臨床試験や製造販売後、診療の場における患者さんへの危害を未然に防止するために不可欠であり、その実施は薬機法等で定められております。当社グループで実施する前臨床試験には、安全性試験(単回・反復投与毒性試験、生殖発生毒性試験等)、薬理試験(安全性薬理試験等)、薬物動態試験があります。各試験の種類や試験内容は次のとおりです。
前臨床試験は、厚生労働省が管轄する薬機法の下、GLP(注2)に従い実施しております。具体的には、運営管理者(注3)が指名した試験責任者(注4)の指揮監督の下で、試験計画書(注5)及び標準操作手順書(SOP)(注6)に従って適切に実施し、その成績を最終報告書(注7)として作成し、委託者へ報告しております。なお、試験がGLPに従い適切に実施されていることについて、信頼性保証部門(注8)が試験全般にわたって客観的に調査することがGLPに定められております。
委託者による試験依頼から最終報告書に至る試験の流れは、次のとおりであります。
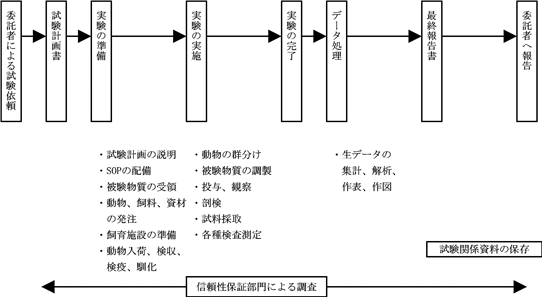 前臨床試験を実施するにあたっては、GLPの厳格な適用並びに技術力を備えた人材の確保に加えて、飼育施設、試験成績の収集・測定・分析・解析等を行う専用機器、資料保存施設等が充分に整った環境及び実験動物の確保が必要不可欠となります。試験の種類に応じた実験を迅速に開始できる体制を整えるべく、経験豊富で高い技術力を備えた研究者の確保、容易に各種実験動物を準備できるだけの検疫施設及び飼育・繁殖体制の整備、研究施設における諸設備の充実等を図っております。
前臨床試験を実施するにあたっては、GLPの厳格な適用並びに技術力を備えた人材の確保に加えて、飼育施設、試験成績の収集・測定・分析・解析等を行う専用機器、資料保存施設等が充分に整った環境及び実験動物の確保が必要不可欠となります。試験の種類に応じた実験を迅速に開始できる体制を整えるべく、経験豊富で高い技術力を備えた研究者の確保、容易に各種実験動物を準備できるだけの検疫施設及び飼育・繁殖体制の整備、研究施設における諸設備の充実等を図っております。
当社グループの前臨床試験においては、ヒトとの遺伝子的類似性が高いことから実験動物の中で最も優位性が高いとされているサルを用いた試験を実施しております。サルを用いた試験は、他の実験動物に比べて取扱いが困難であります。当社では自社開発した保定器具(国際特許取得)を用いることにより、安全に試験実施できることに加え、動物にストレスを与えない状態で試験データ採取が可能で、信頼性の高い試験が実施できます。サルの取扱いは、輸入、検疫、飼育及び繁殖に関する基礎技術・ノウハウを保持している必要があります。加えて、当社敷地内には、農林水産大臣の指定を受けた検疫施設(保税倉庫)があり、実験動物としての品質や安定的数量を確保しております。
(注1)被験物質:試験において安全性の評価の対象となる医薬品又は化学的物質、生物学的物質もしくはその製剤をいいます。
(注2)GLP:Good Laboratory Practiceの略語で、「医薬品の安全性に関する非臨床試験の実施の基準」のことです。医薬品等の製造販売承認申請の際に提出すべき資料のうち、動物による安全性試験データの信頼性を確保するために、試験実施施設が遵守しなくてはならない事項を定めたものです。1979年6月に世界で最初に米国においてGLPが実施され、これを契機として各国において各種のGLPが制定されました。我が国においては、1983年4月に実施された医薬品GLPが始まりで、現在では1996年の旧 薬事法等の一部改正に伴い厚生省令として定められ、1997年4月より施行されました。なお、国内では医薬品GLPの他7種類のGLPが施行されています。
(注3)運営管理者:試験施設の運営及び管理について責任を有する者です。
(注4)試験責任者(SD:Study Director):運営管理者によって各試験毎に指名され、当該試験の計画、実施、記録、報告等について責任を有する者です。
(注5)試験計画書(Protocol):試験の目的を達成するのに必要な試験方法、操作方法が確実に行われるようにするため、試験責任者が試験毎に作成した文書です。
(注6)標準操作手順書(SOP:Standard Operating Procedures):試験が恒常的に適正に実施されるように試験の操作、動物の飼育管理、機器の維持管理等について、実施方法及び手順を記載した文書です。
(注7)最終報告書(Final Report):試験責任者が、試験毎に試験成績を最終的に報告書として作成した文書です。
(注8)信頼性保証部門(QAU:Quality Assurance Unit):信頼性保証部門は、試験の信頼性を保証するための個人又は組織です。信頼性保証部門責任者は運営管理者によって、試験の担当者以外の者から指名されます。さらに、信頼性保証部門責任者は信頼性保証部門担当者を指名し、この信頼性保証部門責任者及び担当者は、客観的な目で試験全般にわたって調査しています。必要に応じて、試験の過程で見られた試験計画書等に従わなかったこと等について指摘、改善を勧告する役割を負っています。その活動の記録、報告は全て文書によって保存されています。
(5) 臨床事業について
前臨床試験の次の段階である臨床試験(治験)は、被験物質のヒトでの有効性と安全性を確認する試験となります。これは、製薬企業等が実施するものと位置付けられておりますが、ヒトでの試験であることから、製薬企業等は医療機関(医師を含む)に治験への参画を依頼することとなります。即ち、製薬企業等が医療機関に治験の実施を依頼し、医療機関がそれを受託することにより実施されます。
実施にあたって、製薬企業等(治験依頼者)は、治験の実施準備として、今までの前臨床試験を含めた成績をまとめて評価し、治験実施計画書(注1)案を作成し、その治験実施計画書案に従った治験ができる医師を選び、医師が所属する医療機関に治験の依頼手続きを行います。依頼を受けた医療機関は、治験実施計画書案が倫理的、科学的、医学的妥当性及び当該医療機関における実施可能性の観点から評価するために、治験実施の可否について治験審査委員会(IRB)(注2)に諮り、実施の承認を得て治験の契約を行います。その後、被験者の同意(インフォームド・コンセント)(注3)を得た上で、GCP(注4)、治験実施計画書、標準業務手順書(SOP)(注5)及び薬機法に従って治験を実施します。治験の結果は、症例報告書(注6)として作成され、治験終了通知書(注7)と共に治験依頼者に提出されて治験が終了します。これらの医療機関での治験の実施に関して、治験依頼者は治験がGCP及び治験実施計画書等に従って実施されていることを確認します。以上のように、治験は、製薬企業等と医療機関との間における様々な専門的な管理・運営の下で行われています。
臨床事業には、主に製薬企業等から臨床試験の管理を受託し、製薬企業の代わりに医療機関に訪問して治験の進捗を管理する事業(CRO事業)並びに治験コーディネーターを派遣して現場での臨床試験を支援する事業(SMO事業)の二つがあります。当社では、関連会社である株式会社新日本科学PPDにおいてCRO事業を行っております。
医療機関における臨床試験(治験)とCRO及びSMOの流れは、次のとおりであります。
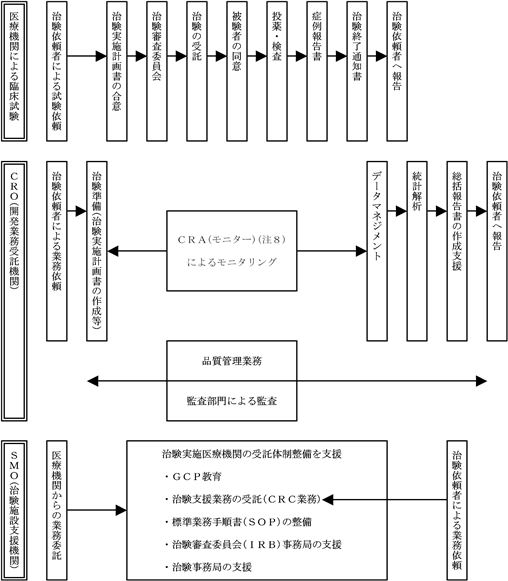 医薬品開発がグローバル化する中で国際競争を展開する製薬企業は、開発のスピードアップを重点課題としており、開発業務をアウトソーシングする動きが活発化し、医療機関では治験体制の整備に関するニーズが高まっております。近年、CRO業界においては、新規参入が相次ぎ競争が激化してきております。当社グループのCROは共に前臨床事業で築き上げた製薬企業等との強い信頼関係を活かして積極的な展開を行っております。
医薬品開発がグローバル化する中で国際競争を展開する製薬企業は、開発のスピードアップを重点課題としており、開発業務をアウトソーシングする動きが活発化し、医療機関では治験体制の整備に関するニーズが高まっております。近年、CRO業界においては、新規参入が相次ぎ競争が激化してきております。当社グループのCROは共に前臨床事業で築き上げた製薬企業等との強い信頼関係を活かして積極的な展開を行っております。
当社は、1999年に臨床開発事業本部(後に臨床事業部と改称)を開設して臨床試験の受託に注力しておりました。近年、臨床試験のCRO市場は、これまでの国内に限定した臨床試験の実施から多国間で同時に行う国際共同試験(以下「グローバル試験」)や日本を含むアジア周辺の複数国で同時に行うアジア試験にトレンドが移りつつある中、グローバル試験を受注するには、世界で同時に臨床試験を運営・管理・実施できる多国間のグローバルネットワークの構築が必須であるところから、いわゆる世界に網羅的に事業所を有するグローバルCRO(注9)とのアライアンスの締結が重要な鍵となっておりました。
こうした背景を踏まえて、当社の臨床事業部門は、グローバル試験のうち日本で実施される試験を受託すべく組織体制の国際化を進め、同時にグローバルCROとの提携を模索していたところ、Pharmaceutical Product Development, LLC.(以下「PPD」)から国内での合弁会社設立の提案を受けました。この提案を受ける形で、当社は、2015年4月1日を効力発生日として当社臨床事業とPPDとの合弁事業会社を設立しました。具体的には、当社(臨床事業)を分割会社とし、PPDの日本子会社ピー・ピー・ディー・ジャパン株式会社を分割承継法人(分割後の商号:株式会社新日本科学PPD)とする会社分割を行いました。両社の日本における臨床事業を統合することで、当社は、グローバル試験の国内実施体制の基盤が強固となり、PPDのグローバルネットワークを活用して、日本国内の臨床試験の受託のみならず、グローバル臨床試験を含む幅広い試験の受託が可能となります。なお、株式会社新日本科学PPDは、当社の持分法適用会社であります。
CROにおける治験支援業務の種類及び業務内容は、次のとおりであります。
(注1)治験実施計画書(Protocol):治験依頼者(製薬企業等)が治験責任医師と協議の上作成するもので、治験の目的、デザイン、方法、統計学的な考察及び組織について記述した文書です。
(注2)治験審査委員会(IRB:Institutional Review Board):治験を実施する医療機関に設置される委員会で、医学、薬学、看護学、法律学、倫理学等の専門家により構成されています。その医療機関が依頼を受けた治験を実施すべきかどうか等について、独立した立場で審査します。
(注3)インフォームド・コンセント(Informed Consent):被験者が、治験の目的や方法等、あらゆる角度から十分な説明がなされた上で、自由な意志によって治験への参加に同意し、書面によってそのことを確認することです。インフォームド・コンセントは、被験者の記名捺印(又は署名)と日付が記入された同意書をもって証明されます。
(注4)GCP:Good Clinical Practiceの略語で、「医薬品の臨床試験の実施の基準」のことです。即ち、医薬品の製造販売承認申請の際に提出すべき資料収集のために行われる臨床試験(治験)を、十分な倫理的配慮のもとに科学的かつ適正に実施するための手順を定めたものです。1989年10月に厚生省薬務局長通知として公表され、翌1990年10月から実施に移されました。その後、より適正な臨床試験の実施と国際調和のために内容を見直された新GCPが、1997年3月に厚生省令として制定、1998年4月から本格施行され、以降適宜改正されております。
(注5)標準業務手順書(SOP:Standard Operating Procedures):治験に係る各々の業務が品質を確保する目的で、恒常的かつ適正に実施されるよう手順を標準化したものです。
(注6)症例報告書(CRF:Case Report Form):治験の成績等を治験依頼者に報告するために、治験実施計画書において規定されている各被験者の全ての情報を記録したものです。
(注7)治験終了通知書:治験終了後に医療機関が作成し、治験依頼者に提出するものです。
(注8)CRA:Clinical Research Associateの略語で、一般的には「モニター」と称します。治験依頼者により指名されたモニターが治験の進行状況を調査し、治験が治験実施計画書、標準業務手順書、薬機法に規定する基準に従って、実施、記録及び報告されることを保証するモニタリング業務を行います。
(注9)グローバルCRO:世界を網羅的にとらえて臨床試験を運営・管理・実施する多国間ネットワークを構築している国際的規模のCROのことを言います。
(6) トランスレーショナル リサーチ(TR)事業について
トランスレーショナル リサーチ(TR: Translational Research)とは、基礎研究から生まれる有望なシーズや新技術を発掘して、医薬品としての評価・承認に必要な前臨床試験や臨床試験を行いながら、基礎理論を臨床の場で実証し、付加価値を高めて事業化へつなげる研究開発です。元来CROである当社グループは、前臨床から臨床までの医薬品開発のプロセスを実施でき、新規技術や物質の評価・事業化するノウハウを有するため、人材面・資金面・経営面で支援を行うこと、さらには独力で創薬を目指すことが可能です。当社TRカンパニーでは、デバイスを含む独自の経鼻投与基盤技術(NDS: Nasal Delivery System)及び薬物の脳移行性を高める独自の送達技術(Nose-to-Brain送達技術)を有しております。当社グループ内の医薬品研究開発機能を活用し、さらにアカデミアとの共同研究も実施しながら、基盤技術を深化させて開発医薬品に応用し、創薬をおこないつつあります。また、これらの基盤技術を応用し当カンパニーよりすでにスピンアウトした、経鼻片頭痛治療薬の開発会社であるSatsuma Pharmaceuticals, Inc.(カリフォルニア州)及び経鼻神経変性疾患レスキュー薬の臨床開発をおこなう株式会社SNLD(日本国内)を支援しています。
(7) メディポリス事業について
メディポリス事業では、地熱発電事業並びにホテル宿泊施設を運営しています。純国産エネルギーの創出推進という国のエネルギー政策をうけて、再生可能エネルギーの固定価格買取制度の施行により、自社保有するメディポリス指宿敷地内に環境に配慮した完全閉鎖式バイナリ―型地熱発電所(1500kw級)を建設し、売電事業を行っております。また、敷地内に建設された一般社団法人メディポリス医学研究所メディポリス国際陽子線治療センターと連携して、自然と健康をテーマにした指宿ベイテラスHOTEL&SPA(2017年7月1日より指宿ベイヒルズHOTEL&SPAに名称変更)を運営しております。また、ホテルの一部を改装・増築し、2020年12月よりヒーリングリゾートホテル「別邸天降る丘」としても運営を開始いたしました。
(8) その他事業について
連結子会社となる特例子会社「ふれあい・ささえあい株式会社」は、身体が不自由な方や精神発達に遅れが出ている方が「働きたい」という思いを実現するために設立した会社です。新日本科学グループ内の業務支援として、清掃、事務、福利厚生(鍼灸師によるマッサージ)などを行っています。
当社グループの企業集団は、当社、連結子会社22社及び関連会社3社の合計26社で構成されております。事業の内容は、1.製薬企業等から前臨床試験(注1)、臨床試験(治験)(注2)(注3)及び新薬承認申請業務を受託し、医薬品開発支援を行うCRO(Contract Research Organization)事業、2.当社が独自に開発した経鼻投与製剤(注4)並びに大学やバイオベンチャーの基礎的な知見や技術を育成してビジネス化していくトランスレーショナル リサーチ(TR)事業、3.メディポリス指宿において地熱発電や宿泊施設運営などを行うメディポリス事業を行っております。
具体的には、CRO事業では、安全性研究所において前臨床試験を、薬物代謝分析センターにおいて前臨床試験及び臨床試験の試料分析を、株式会社新日本科学PPDにおいて臨床試験をそれぞれ受託しております。TR事業としては、薬物の鼻粘膜吸収性を高める独自の経鼻投与基盤技術やデバイス、及び薬物の脳移行性を高める独自の送達技術を研究開発し、これらを応用した創薬を行っております。当事業部よりスピンアウトした経鼻片頭痛治療薬の開発会社である米国Satsuma Pharmaceuticals, Inc.、及び経鼻神経変性疾患レスキュー薬の開発会社である国内株式会社SNLDを支援しています。その他、核酸医薬品の開発を行う米国WAVE Life Sciences Ltd.は当事業部を起源としております。メディポリス事業では、環境に配慮した完全閉鎖式バイナリ―地熱発電事業並びに一般社団法人メディポリス医学研究所メディポリス国際陽子線治療センターと連携して、宿泊施設別邸天降る丘と指宿ベイヒルズHOTEL&SPAを運営しています。
香港の新日本科学(亜州)有限公司は、アジアにおける事業を統括し、中国本土の肇慶創薬生物科技有限公司、カンボジア王国のTIAN HU(CAMBODIA)ANIMAL BREEDING RESEARCH CENTER Ltd.では、実験動物の繁殖育成と検疫輸出を行っています。
(注1)前臨床試験:臨床試験に着手する前に、実験動物や細胞・細菌を用いて医薬品等の化学物質の有効性と安全性を確認する試験です。
(注2)臨床試験:ヒトに対する薬の有効性と安全性を確認するために、医療機関で実施する試験です。
(注3)治験:臨床試験のうち、厚生労働省から新薬の承認を得るために実施する試験です。
(注4)経鼻投与製剤:既に市販されている薬剤の剤型に工夫を施し、鼻から投与し、鼻粘膜から吸収させ、治療するシステムのことであります。
(2) 医薬品開発のプロセスにおける当社グループの事業領域について
製薬企業は、医薬品を開発し、最終的に販売するまでには薬機法に基づく様々な試験を実施し、有効性と安全性を確認します。厚生労働省に新薬承認申請を行うに際しては、それらの試験の成績を添付し、同省諮問機関の専門家による厳密な審査を経て承認が得られるシステムになっております。
医薬品開発のプロセスにおける当社グループの事業領域については、次のとおりであります。
 (3) セグメントについて
(3) セグメントについてセグメントは、当社と連結子会社22社、持分法適用関連会社3社により、次のとおりCRO事業(前臨床事業・臨床事業)・トランスレーショナル リサーチ事業・メディポリス事業及びその他事業に区分されております。
| セグメント | 主な事業の内容 | 構成会社 |
| CRO事業 | (前臨床事業) 製薬企業等の委託者により創製された被験物質について、実験動物や細胞・細菌を用いてその有効性と安全性を確認する事業 (臨床事業) 治験薬のヒトでの有効性と安全性を確認する事業 | 当社 SNBL U.S.A., Ltd. 新日本科学(亜州)有限公司 肇慶創薬生物科技有限公司 SHIN NIPPON BIOMEDICAL LABORATORIES (CAMBODIA) LIMITED ANGKOR PRIMATES CENTER INC. TIAN HU(CAMBODIA) ANIMAL BREEDING RESEARCH CENTER Ltd. University Medicines International, LLC. 株式会社CLINICAL STUDY SUPPORT 株式会社新日本科学PPD(注) |
| トランスレーショナル リサーチ事業 | 経鼻投与製剤等の開発及び大学、バイオベンチャー、研究機関などにおける基礎研究から派生してくる有望なシーズ技術や新規物質を発掘して、医薬品などの評価・承認に必要な前臨床試験や臨床試験を行いながら、基礎理論を臨床の場で実証することにより、付加価値を高めて事業化する事業等 | 当社 株式会社Gemseki Gemseki投資事業有限責任組合 AXIS株式会社 Ruika Therapeutics, Inc. 株式会社SNLD |
| メディポリス事業 | 宿泊施設運営及び地熱発電事業 | 当社 AMAFURU&Co.株式会社(旧 SNBL Nature 株式会社) 株式会社メディポリスエナジー |
| その他事業 | 事務業務受託等 | 当社 株式会社新日本科学グループ 株式会社メディポリス FREESIA HD,INC. SNBLアセットマネジメント株式会社 ふれあい・ささえあい株式会社 Bhutan Fortune株式会社 トランクソリューション株式会社 JRMPC株式会社(注) 株式会社NANA(注) |
(注)持分法適用関連会社であります。
当社及び連結子会社のセグメント系統図並びに会社別事業内容は、次のとおりであります。
<セグメント系統図>
 <会社別事業内容>
<会社別事業内容>| セグメント | 当社(事業部) 及び主な連結子会社 | 所在地 | 事業内容 | |
| 当社 | CRO事業 | 安全性研究所 | 鹿児島 | 前臨床試験を行っております。 |
| 薬物代謝分析センター | 和歌山 | 前臨床試験及び臨床試験の試料分析を行っております。 | ||
| トランスレーショナルリサーチ事業 | TRカンパニー | 東京・鹿児島 | 経鼻投与製剤等の開発を行っております。 また、大学等との共同研究の推進、バイオベンチャー等の支援を行っております。 | |
| メディポリス 事業 | 別邸天降る丘 | 鹿児島 | ホテル宿泊施設を運営しております。 | |
| 発電事業部 | 鹿児島 | 地熱発電事業等を行っております。 | ||
| 主な 連結 子会社 | CRO事業 | 肇慶創薬生物科技有限公司 | 中国広東省 | 実験動物の繁殖・育成・検疫等を行っております。 |
| SHIN NIPPON BIOMEDICAL LABORATORIES (CAMBODIA) LIMITED | カンボジア王国プノンペン都 | 実験動物の繁殖・育成・検疫等を行っております。 | ||
| トランスレーショナルリサーチ事業 | 株式会社Gemseki | 東京 | 知財仲介事業及びファンド運営を行っております。 | |
| 株式会社SNLD | 東京 | 経鼻投与製剤の開発を行っております。 | ||
| メディポリス 事業 | 株式会社メディポリスエナジー | 鹿児島 | 地熱発電事業を行っております。 |
(4) 前臨床事業について
前臨床試験とは、製薬企業等により開発された被験物質(注1)の有効性と安全性について、実験動物や細胞・細菌などを用いて調べる試験です。実験動物を用いる前臨床試験は、その後に続く、ヒトによる臨床試験や製造販売後、診療の場における患者さんへの危害を未然に防止するために不可欠であり、その実施は薬機法等で定められております。当社グループで実施する前臨床試験には、安全性試験(単回・反復投与毒性試験、生殖発生毒性試験等)、薬理試験(安全性薬理試験等)、薬物動態試験があります。各試験の種類や試験内容は次のとおりです。
| 前臨床試験の種類 | 説明 | |
| 安全性試験 | 単回投与毒性試験 | 被験物質を単回投与し、その毒性を質的量的に明らかにする試験です。 |
| 反復投与毒性試験 | 被験物質を繰り返し投与したとき、明らかな毒性変化を示す用量とその変化の内容及び毒性変化の認められない用量を求める試験です。 | |
| 生殖発生毒性試験 | 被験物質の生体への適用が、生殖・発生の過程において何らかの悪影響を及ぼすかどうかの情報を得ることを目的とした試験です。 | |
| 抗原性試験 | 薬物がヒトに対して免疫反応に関与する副作用を起こす可能性があるかどうかを調べる試験です。 | |
| 皮膚(光)感作性試験 | 皮膚外用剤として用いる医薬品の皮膚での接触感作性、皮膚光感作性のリスクを予測するための試験です。 | |
| 遺伝毒性試験 | 細胞や細菌を用いて、被験物質の遺伝子突然変異誘発性や染色体異常誘発性を推定する試験です。 | |
| がん原性試験 | 被験物質が、がん原性を示すかを調べる試験です。 | |
| 局所刺激性試験 | 被験物質を局所に適用し、その刺激性を調べる試験です。 | |
| 吸入毒性試験 | 吸入装置を用いて、被験物質を全身に暴露した場合、あるいは口や鼻から吸入した場合の毒性を調べる試験です。 | |
| TK試験 | 被験物質を投与した際の血漿あるいは血清中の薬物の濃度を測定し、全身的暴露量を経時的に調べる試験です。 | |
| 特性試験 | 被験物質の特性として、純度、含量や性状等を調べる試験です。 | |
| 安定性試験 | 被験物質の安定性を調べる試験です。 | |
| 薬理試験 | 安全性薬理試験 | 薬物の薬理作用又は副作用の観察を目的として、ヒトでの安全性を予測するために行われる試験です。 |
| 薬効試験 | 薬物の有効性を評価することを目的として行われる試験です。 | |
| 薬物動態試験 | 被験物質投与後の生体内での被験物質及びその代謝物の時間経過に伴う吸収、分布、代謝、排泄等について調べる試験です。 | |
前臨床試験は、厚生労働省が管轄する薬機法の下、GLP(注2)に従い実施しております。具体的には、運営管理者(注3)が指名した試験責任者(注4)の指揮監督の下で、試験計画書(注5)及び標準操作手順書(SOP)(注6)に従って適切に実施し、その成績を最終報告書(注7)として作成し、委託者へ報告しております。なお、試験がGLPに従い適切に実施されていることについて、信頼性保証部門(注8)が試験全般にわたって客観的に調査することがGLPに定められております。
委託者による試験依頼から最終報告書に至る試験の流れは、次のとおりであります。
 前臨床試験を実施するにあたっては、GLPの厳格な適用並びに技術力を備えた人材の確保に加えて、飼育施設、試験成績の収集・測定・分析・解析等を行う専用機器、資料保存施設等が充分に整った環境及び実験動物の確保が必要不可欠となります。試験の種類に応じた実験を迅速に開始できる体制を整えるべく、経験豊富で高い技術力を備えた研究者の確保、容易に各種実験動物を準備できるだけの検疫施設及び飼育・繁殖体制の整備、研究施設における諸設備の充実等を図っております。
前臨床試験を実施するにあたっては、GLPの厳格な適用並びに技術力を備えた人材の確保に加えて、飼育施設、試験成績の収集・測定・分析・解析等を行う専用機器、資料保存施設等が充分に整った環境及び実験動物の確保が必要不可欠となります。試験の種類に応じた実験を迅速に開始できる体制を整えるべく、経験豊富で高い技術力を備えた研究者の確保、容易に各種実験動物を準備できるだけの検疫施設及び飼育・繁殖体制の整備、研究施設における諸設備の充実等を図っております。当社グループの前臨床試験においては、ヒトとの遺伝子的類似性が高いことから実験動物の中で最も優位性が高いとされているサルを用いた試験を実施しております。サルを用いた試験は、他の実験動物に比べて取扱いが困難であります。当社では自社開発した保定器具(国際特許取得)を用いることにより、安全に試験実施できることに加え、動物にストレスを与えない状態で試験データ採取が可能で、信頼性の高い試験が実施できます。サルの取扱いは、輸入、検疫、飼育及び繁殖に関する基礎技術・ノウハウを保持している必要があります。加えて、当社敷地内には、農林水産大臣の指定を受けた検疫施設(保税倉庫)があり、実験動物としての品質や安定的数量を確保しております。
(注1)被験物質:試験において安全性の評価の対象となる医薬品又は化学的物質、生物学的物質もしくはその製剤をいいます。
(注2)GLP:Good Laboratory Practiceの略語で、「医薬品の安全性に関する非臨床試験の実施の基準」のことです。医薬品等の製造販売承認申請の際に提出すべき資料のうち、動物による安全性試験データの信頼性を確保するために、試験実施施設が遵守しなくてはならない事項を定めたものです。1979年6月に世界で最初に米国においてGLPが実施され、これを契機として各国において各種のGLPが制定されました。我が国においては、1983年4月に実施された医薬品GLPが始まりで、現在では1996年の旧 薬事法等の一部改正に伴い厚生省令として定められ、1997年4月より施行されました。なお、国内では医薬品GLPの他7種類のGLPが施行されています。
(注3)運営管理者:試験施設の運営及び管理について責任を有する者です。
(注4)試験責任者(SD:Study Director):運営管理者によって各試験毎に指名され、当該試験の計画、実施、記録、報告等について責任を有する者です。
(注5)試験計画書(Protocol):試験の目的を達成するのに必要な試験方法、操作方法が確実に行われるようにするため、試験責任者が試験毎に作成した文書です。
(注6)標準操作手順書(SOP:Standard Operating Procedures):試験が恒常的に適正に実施されるように試験の操作、動物の飼育管理、機器の維持管理等について、実施方法及び手順を記載した文書です。
(注7)最終報告書(Final Report):試験責任者が、試験毎に試験成績を最終的に報告書として作成した文書です。
(注8)信頼性保証部門(QAU:Quality Assurance Unit):信頼性保証部門は、試験の信頼性を保証するための個人又は組織です。信頼性保証部門責任者は運営管理者によって、試験の担当者以外の者から指名されます。さらに、信頼性保証部門責任者は信頼性保証部門担当者を指名し、この信頼性保証部門責任者及び担当者は、客観的な目で試験全般にわたって調査しています。必要に応じて、試験の過程で見られた試験計画書等に従わなかったこと等について指摘、改善を勧告する役割を負っています。その活動の記録、報告は全て文書によって保存されています。
(5) 臨床事業について
前臨床試験の次の段階である臨床試験(治験)は、被験物質のヒトでの有効性と安全性を確認する試験となります。これは、製薬企業等が実施するものと位置付けられておりますが、ヒトでの試験であることから、製薬企業等は医療機関(医師を含む)に治験への参画を依頼することとなります。即ち、製薬企業等が医療機関に治験の実施を依頼し、医療機関がそれを受託することにより実施されます。
実施にあたって、製薬企業等(治験依頼者)は、治験の実施準備として、今までの前臨床試験を含めた成績をまとめて評価し、治験実施計画書(注1)案を作成し、その治験実施計画書案に従った治験ができる医師を選び、医師が所属する医療機関に治験の依頼手続きを行います。依頼を受けた医療機関は、治験実施計画書案が倫理的、科学的、医学的妥当性及び当該医療機関における実施可能性の観点から評価するために、治験実施の可否について治験審査委員会(IRB)(注2)に諮り、実施の承認を得て治験の契約を行います。その後、被験者の同意(インフォームド・コンセント)(注3)を得た上で、GCP(注4)、治験実施計画書、標準業務手順書(SOP)(注5)及び薬機法に従って治験を実施します。治験の結果は、症例報告書(注6)として作成され、治験終了通知書(注7)と共に治験依頼者に提出されて治験が終了します。これらの医療機関での治験の実施に関して、治験依頼者は治験がGCP及び治験実施計画書等に従って実施されていることを確認します。以上のように、治験は、製薬企業等と医療機関との間における様々な専門的な管理・運営の下で行われています。
臨床事業には、主に製薬企業等から臨床試験の管理を受託し、製薬企業の代わりに医療機関に訪問して治験の進捗を管理する事業(CRO事業)並びに治験コーディネーターを派遣して現場での臨床試験を支援する事業(SMO事業)の二つがあります。当社では、関連会社である株式会社新日本科学PPDにおいてCRO事業を行っております。
医療機関における臨床試験(治験)とCRO及びSMOの流れは、次のとおりであります。
 医薬品開発がグローバル化する中で国際競争を展開する製薬企業は、開発のスピードアップを重点課題としており、開発業務をアウトソーシングする動きが活発化し、医療機関では治験体制の整備に関するニーズが高まっております。近年、CRO業界においては、新規参入が相次ぎ競争が激化してきております。当社グループのCROは共に前臨床事業で築き上げた製薬企業等との強い信頼関係を活かして積極的な展開を行っております。
医薬品開発がグローバル化する中で国際競争を展開する製薬企業は、開発のスピードアップを重点課題としており、開発業務をアウトソーシングする動きが活発化し、医療機関では治験体制の整備に関するニーズが高まっております。近年、CRO業界においては、新規参入が相次ぎ競争が激化してきております。当社グループのCROは共に前臨床事業で築き上げた製薬企業等との強い信頼関係を活かして積極的な展開を行っております。当社は、1999年に臨床開発事業本部(後に臨床事業部と改称)を開設して臨床試験の受託に注力しておりました。近年、臨床試験のCRO市場は、これまでの国内に限定した臨床試験の実施から多国間で同時に行う国際共同試験(以下「グローバル試験」)や日本を含むアジア周辺の複数国で同時に行うアジア試験にトレンドが移りつつある中、グローバル試験を受注するには、世界で同時に臨床試験を運営・管理・実施できる多国間のグローバルネットワークの構築が必須であるところから、いわゆる世界に網羅的に事業所を有するグローバルCRO(注9)とのアライアンスの締結が重要な鍵となっておりました。
こうした背景を踏まえて、当社の臨床事業部門は、グローバル試験のうち日本で実施される試験を受託すべく組織体制の国際化を進め、同時にグローバルCROとの提携を模索していたところ、Pharmaceutical Product Development, LLC.(以下「PPD」)から国内での合弁会社設立の提案を受けました。この提案を受ける形で、当社は、2015年4月1日を効力発生日として当社臨床事業とPPDとの合弁事業会社を設立しました。具体的には、当社(臨床事業)を分割会社とし、PPDの日本子会社ピー・ピー・ディー・ジャパン株式会社を分割承継法人(分割後の商号:株式会社新日本科学PPD)とする会社分割を行いました。両社の日本における臨床事業を統合することで、当社は、グローバル試験の国内実施体制の基盤が強固となり、PPDのグローバルネットワークを活用して、日本国内の臨床試験の受託のみならず、グローバル臨床試験を含む幅広い試験の受託が可能となります。なお、株式会社新日本科学PPDは、当社の持分法適用会社であります。
CROにおける治験支援業務の種類及び業務内容は、次のとおりであります。
| 業務の種類 | 業務の内容 |
| 治験薬概要書の作成支援 | 前臨床試験成績及び先行して実施された臨床試験成績に基づいてまとめた的確な治験薬概要書の作成を支援しております。 |
| 治験実施計画書の作成支援 | 治験の目的、デザイン、方法、統計学的な考察及び組織について記述した文書の作成を支援しております。 |
| 同意説明文書の作成支援 | 被験者から治験の参加に関する同意を得るために用いる文書の作成を支援しております。 |
| 治験責任医師の選定 治験実施医療機関の選定 | 治験を適切に実施できる治験責任医師及び実施医療機関を選定する業務です。 |
| 治験薬割付 | 治験薬の評価にバイアスを避けるために治験薬が特定できないようにする業務です。通常、記号と算用数字を組み合わせて、あるいは算用数字で表示します。 |
| 治験の依頼・契約 | 医療機関への治験の依頼及び契約をする業務です。 |
| モニタリング | 治験依頼者により指名されたモニターが、治験の進行状況を調査し、GCP及び治験実施計画書、標準業務手順書に従って、実施、記録及び報告されていることを保証する業務です。 |
| 品質管理 | 治験の品質管理を目的として行う点検業務です。 |
| データマネジメント(DM:Data Management) | 治験データの確認業務のことで、DM業務担当者は、モニターが治験責任医師から入手した症例報告書の内容を確認して、治験実施計画書に定める事項からの逸脱、記入漏れ、不整合等を発見し、モニターを通じて治験責任医師にフィードバックします。データを固定後、統計解析業務担当者に提供する業務です。 |
| 統計解析業務 | データマネジメント業務を通じて作成されたデータベースを用いて治験実施計画書に定めた統計手法に基づき有効性、安全性の統計解析を行う業務です。 |
| 総括報告書の作成支援 | 治験の終了後、治験の目的、方法及び成績等をまとめた治験に関する報告書の作成を支援しております。 |
| 電子申請支援 | 各種申請を支援しております。 |
| 官公庁への申請書類提出支援 | 官公庁への各種申請書類の作成や手続きを支援しております。 |
| 薬事コンサルティング | 新薬の開発から申請、承認、製造販売後までにわたる様々な薬事コンサルティング業務です。 |
(注1)治験実施計画書(Protocol):治験依頼者(製薬企業等)が治験責任医師と協議の上作成するもので、治験の目的、デザイン、方法、統計学的な考察及び組織について記述した文書です。
(注2)治験審査委員会(IRB:Institutional Review Board):治験を実施する医療機関に設置される委員会で、医学、薬学、看護学、法律学、倫理学等の専門家により構成されています。その医療機関が依頼を受けた治験を実施すべきかどうか等について、独立した立場で審査します。
(注3)インフォームド・コンセント(Informed Consent):被験者が、治験の目的や方法等、あらゆる角度から十分な説明がなされた上で、自由な意志によって治験への参加に同意し、書面によってそのことを確認することです。インフォームド・コンセントは、被験者の記名捺印(又は署名)と日付が記入された同意書をもって証明されます。
(注4)GCP:Good Clinical Practiceの略語で、「医薬品の臨床試験の実施の基準」のことです。即ち、医薬品の製造販売承認申請の際に提出すべき資料収集のために行われる臨床試験(治験)を、十分な倫理的配慮のもとに科学的かつ適正に実施するための手順を定めたものです。1989年10月に厚生省薬務局長通知として公表され、翌1990年10月から実施に移されました。その後、より適正な臨床試験の実施と国際調和のために内容を見直された新GCPが、1997年3月に厚生省令として制定、1998年4月から本格施行され、以降適宜改正されております。
(注5)標準業務手順書(SOP:Standard Operating Procedures):治験に係る各々の業務が品質を確保する目的で、恒常的かつ適正に実施されるよう手順を標準化したものです。
(注6)症例報告書(CRF:Case Report Form):治験の成績等を治験依頼者に報告するために、治験実施計画書において規定されている各被験者の全ての情報を記録したものです。
(注7)治験終了通知書:治験終了後に医療機関が作成し、治験依頼者に提出するものです。
(注8)CRA:Clinical Research Associateの略語で、一般的には「モニター」と称します。治験依頼者により指名されたモニターが治験の進行状況を調査し、治験が治験実施計画書、標準業務手順書、薬機法に規定する基準に従って、実施、記録及び報告されることを保証するモニタリング業務を行います。
(注9)グローバルCRO:世界を網羅的にとらえて臨床試験を運営・管理・実施する多国間ネットワークを構築している国際的規模のCROのことを言います。
(6) トランスレーショナル リサーチ(TR)事業について
トランスレーショナル リサーチ(TR: Translational Research)とは、基礎研究から生まれる有望なシーズや新技術を発掘して、医薬品としての評価・承認に必要な前臨床試験や臨床試験を行いながら、基礎理論を臨床の場で実証し、付加価値を高めて事業化へつなげる研究開発です。元来CROである当社グループは、前臨床から臨床までの医薬品開発のプロセスを実施でき、新規技術や物質の評価・事業化するノウハウを有するため、人材面・資金面・経営面で支援を行うこと、さらには独力で創薬を目指すことが可能です。当社TRカンパニーでは、デバイスを含む独自の経鼻投与基盤技術(NDS: Nasal Delivery System)及び薬物の脳移行性を高める独自の送達技術(Nose-to-Brain送達技術)を有しております。当社グループ内の医薬品研究開発機能を活用し、さらにアカデミアとの共同研究も実施しながら、基盤技術を深化させて開発医薬品に応用し、創薬をおこないつつあります。また、これらの基盤技術を応用し当カンパニーよりすでにスピンアウトした、経鼻片頭痛治療薬の開発会社であるSatsuma Pharmaceuticals, Inc.(カリフォルニア州)及び経鼻神経変性疾患レスキュー薬の臨床開発をおこなう株式会社SNLD(日本国内)を支援しています。
(7) メディポリス事業について
メディポリス事業では、地熱発電事業並びにホテル宿泊施設を運営しています。純国産エネルギーの創出推進という国のエネルギー政策をうけて、再生可能エネルギーの固定価格買取制度の施行により、自社保有するメディポリス指宿敷地内に環境に配慮した完全閉鎖式バイナリ―型地熱発電所(1500kw級)を建設し、売電事業を行っております。また、敷地内に建設された一般社団法人メディポリス医学研究所メディポリス国際陽子線治療センターと連携して、自然と健康をテーマにした指宿ベイテラスHOTEL&SPA(2017年7月1日より指宿ベイヒルズHOTEL&SPAに名称変更)を運営しております。また、ホテルの一部を改装・増築し、2020年12月よりヒーリングリゾートホテル「別邸天降る丘」としても運営を開始いたしました。
(8) その他事業について
連結子会社となる特例子会社「ふれあい・ささえあい株式会社」は、身体が不自由な方や精神発達に遅れが出ている方が「働きたい」という思いを実現するために設立した会社です。新日本科学グループ内の業務支援として、清掃、事務、福利厚生(鍼灸師によるマッサージ)などを行っています。