有価証券届出書(新規公開時)
対処すべき課題
文中の将来に関する事項は、本書提出日現在において、当社が判断したものであります。
(1)経営方針
当社は「Create the Future to Overcome Cancer」「がんを克服できる社会の創生に貢献する」という経営理念の下、がん治療とがん免疫療法の現状と課題を熟知した医師達が、「No illness(がんという病を根絶させたい)」「No immunity, No life(免疫なくして生命は成り立たず)」という想いより、2015年4月に「ノイルイミューン・バイオテック」という社名にて当社を創業しました。PRIME技術という革新的な治療プラットフォームを利用した効果的ながん治療法を開発し、多くの患者へ届け、がんを克服した社会の実現に貢献してまいります。
(2)経営戦略
革新性の高いPRIME技術を中核として、ライセンス又は販売による大型の収入が期待でき高い成長性を持つ「自社創薬」と、多数の契約候補先・パイプライン候補・収益機会候補を持ち早期の収益確保が可能な「共同パイプライン」の2つの創薬ビジネスモデルを組み合わせることにより、安定感のある事業ポートフォリオを構成していきます。
一般的に創薬バイオベンチャーは自社パイプラインの開発のために先行投資がかさみ損益分岐点が高く、黒字化が遅れる場合がありますが、当社はPRIME技術による「共同パイプライン」を併せ持つため、より早期の黒字化を可能としていく戦略を選択しております。
「自社創薬」においては、当社においてNIB101の第Ⅰ相臨床試験を進めております。当社で現在開発中のCAR-T製剤は、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(以下、薬機法)上の再生医療等製品に該当するものであるところ、再生医療等製品については、同法に基づき、有効性が推定され、安全性が認められた場合には、その適正な使用の確保のために必要な条件及び7年を超えない範囲内の期限付きで、かつ期限内に改めて製造販売承認を得ることを条件として早期に製造販売承認を得られる可能性があるため、当社が開発中のCAR-T製剤についても、かかる制度を利用して日本における早期の承認を取得し、早期のPOC確立と先行投資の回収を行うことを企図しております。また、武田薬品工業の100%子会社であるMillennium Pharmaceuticals, Inc.との提携により、NIB102及びNIB103についても、第Ⅰ相臨床試験を開始しています。当社は、当該提携の経験を活かし、今後もグローバルの開発、製造、販売経路を有する大手製薬企業とライセンス契約を締結することで、新たな標的抗原の開発も含め、より大きな市場シェアと収益を狙っていきます。
「共同パイプライン」については、既に複数の国内外の大手製薬企業と提携を行っておりますが、これらの経験を活かし、今後も多数の製薬企業とライセンス契約することで、PRIME技術の第三者による技術評価を確立させるとともに、多数のパイプラインを開発することによるリスクヘッジ及び多様な収益形態の収益機会を得ることによる収益基盤の安定化を図ります。
また、当社による医薬品の研究開発においては、PRIME技術に関するものを中心とした知的財産権やノウハウが重要な経営資源となります。当社は、事業の運営及び拡大に必要な特許権等の知的財産権を、国内外において適時適切に出願及び登録することにより、知的財産権の保護の最大化を図る方針です。当社が出願人である又は当社がライセンスを有する登録済もしくは出願中の特許については、上記「第1 企業の概況 3 事業の内容 (8)知的財産権(特許等)について」をご参照ください。
当社は、その経験とPRIME技術を活かし、固形がんに対する次世代細胞療法を開発すべく、技術、創薬、製造、そして人材の確保と定着に継続的に投資することを通じて、最適な標的抗原の選定を含め、新たな分野である固形がんに対する遺伝子改変免疫細胞療法の研究開発を推し進めることにより、固形がん治療の領域における当社のプレゼンスの向上・確立を図ります。
(3)経営上の目標の達成状況を把握するための客観的な指標等
当社は、現在研究開発段階にあり、売上高、利益率、ROA/ROEその他の数値的な目標となる経営指標等は用いておりません。当社は、「自社創薬」と「共同パイプライン」のハイブリッドビジネスモデルに基づき、PRIME技術の市場への展開や周知を加速化して早期の収益確保を図ると同時に、長期的には大型の販売収益を確保することにより、事業経営におけるリスク分散及びサステナブルな事業成長を実現することを目指し、当社の開発パイプライン及び他社との共同プロジェクトの進捗及びより一層のパイプラインの拡充を目標として事業活動を推進しています。開発中の自社パイプラインについて、非臨床試験の段階においては開発段階を詳細に区切った作業工程表を作成しており、定期的なモニタリングを行い開発の進捗状況を適宜確認し管理しております。第I相臨床試験など臨床試験においては、医療機関での治験実施の患者数等を目標管理しております。
共同パイプラインについては、提携した製薬企業等からの定期的な報告を受け、開発の進捗状況を適宜確認しております。
(4)経営環境
①がん罹患率・生存率について
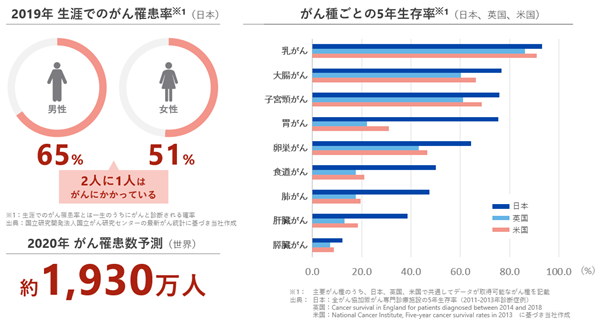
日本国内において、がんの死亡数と罹患数は、人口の高齢化を主な要因としてともに増加し続けております。男女ともがんの死亡数は増加し続けており、2021年のがん死亡数は、38万人以上と報告されております(出典:国立がん研究センターがん情報サービス「がん統計」(厚生労働省人口動態統計))。同様に、男女ともにがんの罹患数は1985年以降増加し続けており、2019年のがん罹患数は99万人以上と報告されております(国立がん研究センターがん情報サービス「がん統計」(全国がん登録))。また、日本人が生涯でがんに罹患する確率は、男性で65%、女性で51%と報告されており、(出典:国立がん研究センターがん情報サービス「がん統計」(累積罹患リスク(グラフデータベース)))、世界の2020年がん罹患者数は約1,930万人(出典:GLOBOCAN 2020)とされております。また、各がん腫の5年生存率は、特にステージの進んだがんにおいて依然として低く、有効な治療法の開発が急務であります。
 ②遺伝子改変免疫細胞療法の市場について
②遺伝子改変免疫細胞療法の市場について
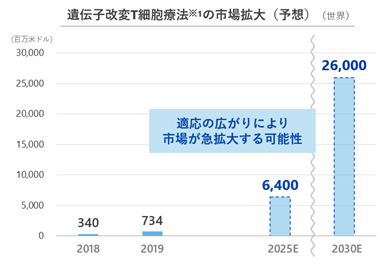
がんによる死亡数は、2020年において世界で約996万人とされております(WHO CANCER Tomorrow)。世界におけるがん治療薬の市場規模は拡大傾向にあり、2018年にはがん免疫療法の研究開発に対してノーベル生理学・医学賞が授与されたこともあり、がん免疫療法に対する期待が大いに高まっております。さらに、最先端のがん免疫療法として遺伝子改変免疫細胞療法が製薬業界で存在感を高めており、CAR-T細胞を代表とする遺伝子改変T細胞療法の世界市場は2030年において260億ドルに達するとも予測されております(国立研究開発法人科学技術振興機構 戦略プロポーザル「デザイナー細胞」)。
③薬価の動向について
CAR-T細胞療法は、固形がんに対する治療法として上市されたものは現時点では存在しないものの、再発又は難治性のB細胞性急性リンパ芽球性白血病やびまん性大細胞型B細胞リンパ腫といった血液がんに対する治療法として実用化されており、スイスの大手製薬企業のノバルティスファーマが開発したキムリア(一般名:チサゲンレクルユーセル)は、高い完全寛解率(※1)と比較的長期の寛解維持(※2)が臨床試験で実証され、医薬品として2017年8月に米国承認、2018年8月に欧州承認、2019年3月に日本承認となりました。米国での薬価は475,000ドル(約5,200万円)、日本での薬価は3,349万円(収載時の薬価。その後の改定により2021年7月時点では3,264万円)と決定されました。また、日本においては、イエスカルタ(一般名:アキシカブタゲン シロルユーセル)とブレンヤンジ(一般名:リソカブタゲン マラルユーセル)が再発又は難治性の大細胞型B細胞リンパ腫に対して承認されており、アベクマ(一般名:イデカブタゲン ビクルユーセル)が再発又は難治性の多発性骨髄腫に対して承認されています。薬価はキムリアと同額となっております。
※1 完全寛解率:全てのがん病変が消失した患者の割合
※2 寛解維持:全てのがん病変が消失し、再発が確認されていない状態
④希少疾病用品目・先駆的品目の指定制度や早期承認制度等について
厚生労働省が2015年度より試行的に実施していた先駆け審査指定制度は、薬機法において先駆的品目の指定制度として法制化され、2020年9月より施行されております。これは、一定の要件を満たす画期的な医薬品等について、開発の比較的早期の段階から先駆的品目指定制度の対象品目に指定し、薬事承認に関する相談・審査における優先的な取扱いをするものです。加えて、薬機法においては、対象となる患者数が少ないために開発のインセンティブが小さい医薬品等について、一定の要件を満たす場合に、希少疾病用品目としての指定を受けることができるとされております。希少疾病用品目として指定を受けた場合には、優先審査の対象となるほか、助成金の交付や税制上の優遇措置等を受けることができ、これにより、希少疾病に関する医薬品等の開発にインセンティブを付与し、そのアンメットメディカルニーズを解消することが企図されています。当社で現在開発中のCAR-T製剤は、これらの指定制度の対象となりうる品目であることから、当社は研究開発を迅速化させるため、これらの指定制度(海外における同様の制度を含みます。)を活用する可能性があります。
また、当社で現在開発中のCAR-T製剤は、薬機法上の再生医療等製品に該当するものであり、その性質上、製品の有効性を確認するための臨床データの収集、評価に長期間を要する場合があります。他方で、再生医療等製品には条件及び期限付承認制度が存在し、限られた数の症例から有効性が推定でき、安全性が確認された場合には、その適正な使用の確保のために必要な条件及び7年を超えない範囲内の期限付きの承認を得られる可能性があります。
⑤CAR-T細胞療法のグローバルでの開発競争の現状
革新的ながん治療法であるCAR-TやTCR-Tといった遺伝子改変免疫細胞療法はグローバルで開発競争が過熱しており、大手製薬メーカーでは自社での内部開発から他社との共同開発、又は買収による研究開発のスピードアップ戦略に切り替える事例も出始めております。海外のCAR-T研究開発を行うベンチャー企業の大型の買収事例も増えており、2017年8月に米ギリアド・サイエンシズがカイトファーマを約119億ドル(約1兆5,289億円)で買収、2018年1月には米セルジーンがジュノ・セラピューティクスを約90億ドル(約1兆1,563億円)で買収しました。また、近年では特に固形がんの治療を対象に、新たな技術を用いたCAR-T細胞療法の開発を実施するベンチャー企業が国内外で精力的に研究開発を実施しております。中でも当社のPRIME技術はCAR-T細胞を強化するだけでなく体内の免疫も誘導するユニークな技術であります。
(5)優先的に対処すべき事業上及び財務上の課題
当社は、固形がんに対する遺伝子改変免疫細胞療法の研究開発を推進すべく、以下の取組みを進めております。
①PRIME技術の基礎研究体制の拡大及び国内外の学術機関、民間機関等との共同研究開発の推進
当社は、山口大学との共同研究等に基づくPRIME技術の活用により、これまで複数のパイプラインを構築しております。また、中核技術であるPRIME技術の改良や応用についての基礎研究を進めております。今後も山口大学との緊密な連携や国内外の学術機関、民間機関等との共同研究開発により、より一層のパイプラインの拡充、及びPRIME技術の周辺知財の構築を図る方針であり、研究体制の拡充を図って参ります。
②臨床試験の推進
当社は、複数のパイプラインを構築しております。そのうち自社創薬のパイプラインであるNIB101について現在第Ⅰ相臨床試験を実施中であり、当該パイプラインの臨床試験を自社主導で推進し、臨床試験より得られたデータを評価することで、ライセンス先における開発の加速にも資するものと考えております。自社パイプラインで最も進捗しているNIB101については、今後も臨床試験を着実に実施して参ります。
③ライセンス先に対する支援
PRIME技術のライセンス契約を締結した製薬企業に対し、臨床開発が滞りなく進められるよう、当社が技術的アドバイスを行い、また、契約によっては分担業務を行い、ライセンス先との協力を継続的に行っていく方針であります。
④ライセンス契約の拡大に向けた体制拡充
安定した事業ポートフォリオの構築とさらなる収益機会の獲得を目指すため、また「共同パイプライン」におけるライセンス契約をより多くの国内外の製薬企業に広めるため、事業開発人材等の適切な人材の拡充が重要であり、外部人材の確保や人材登用等による人材育成及び活用を図って参ります。
⑤新しい事業機会を得るための外部機関との新たな連携
当社は、パイプライン拡充とともに、新たな形態のパイプラインの構築や、細胞医薬製造の効率化を目指しております。そのため、新たなゲノム編集技術や、遺伝子導入法、自動培養装置などの技術を持つ外部機関との連携の拡大を図っております。
⑥財務基盤の強化
当社はこれまで数度にわたるエクイティファイナンスやパートナー企業からのライセンスに関する収入により資金を調達してまいりましたが、今後さらなる研究開発の推進のため、必要に応じて適切な時期に資金調達を実施し、財務的基盤の強化を図ります。
⑦当社の正社員の採用、育成、登用
当社の主要な業務は、原則として正社員によって運用することを基本方針としております。その理由は、当社の経営理念に深く共感する当社のチームメンバーが、主体性をもって研究開発を行うこと、また、ライセンス先の製薬企業と接することが、事業推進の品質とスピードを向上させ、競合他社に対して大きな差別化の要素となり、当業界における最も優れた競争優位性であると考えているためです。
当社への入社志望者については、それまでの経歴や能力、潜在性を評価・選考し、最終面接時に当社の経営理念の説明を行い、候補者にとって共感できているかどうかを、当社の採用基準としております。採用後の育成については、現場での上長によるOJT(オン・ザ・ジョブ・トレーニング)や、部門長によって個人別に計画した教育研修スケジュールを実施しております。
社内登用については、事前に策定した個人別の目標管理シートに基づいて一定の成果をあげているかどうかを確認し、さらに重ねて当社の経営理念に沿った日常的な行動規範をしているかどうかについて、人事評価委員会による評価会議を経て、部門配置や昇格・昇給及び降格・降給を決定しております。
今後も上記の方法に基づき、研究開発の加速パイプラインの進捗等に対応し、必要に応じて適切かつ十分な人材確保に努めてまいります。
(1)経営方針
当社は「Create the Future to Overcome Cancer」「がんを克服できる社会の創生に貢献する」という経営理念の下、がん治療とがん免疫療法の現状と課題を熟知した医師達が、「No illness(がんという病を根絶させたい)」「No immunity, No life(免疫なくして生命は成り立たず)」という想いより、2015年4月に「ノイルイミューン・バイオテック」という社名にて当社を創業しました。PRIME技術という革新的な治療プラットフォームを利用した効果的ながん治療法を開発し、多くの患者へ届け、がんを克服した社会の実現に貢献してまいります。
(2)経営戦略
革新性の高いPRIME技術を中核として、ライセンス又は販売による大型の収入が期待でき高い成長性を持つ「自社創薬」と、多数の契約候補先・パイプライン候補・収益機会候補を持ち早期の収益確保が可能な「共同パイプライン」の2つの創薬ビジネスモデルを組み合わせることにより、安定感のある事業ポートフォリオを構成していきます。
一般的に創薬バイオベンチャーは自社パイプラインの開発のために先行投資がかさみ損益分岐点が高く、黒字化が遅れる場合がありますが、当社はPRIME技術による「共同パイプライン」を併せ持つため、より早期の黒字化を可能としていく戦略を選択しております。
「自社創薬」においては、当社においてNIB101の第Ⅰ相臨床試験を進めております。当社で現在開発中のCAR-T製剤は、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(以下、薬機法)上の再生医療等製品に該当するものであるところ、再生医療等製品については、同法に基づき、有効性が推定され、安全性が認められた場合には、その適正な使用の確保のために必要な条件及び7年を超えない範囲内の期限付きで、かつ期限内に改めて製造販売承認を得ることを条件として早期に製造販売承認を得られる可能性があるため、当社が開発中のCAR-T製剤についても、かかる制度を利用して日本における早期の承認を取得し、早期のPOC確立と先行投資の回収を行うことを企図しております。また、武田薬品工業の100%子会社であるMillennium Pharmaceuticals, Inc.との提携により、NIB102及びNIB103についても、第Ⅰ相臨床試験を開始しています。当社は、当該提携の経験を活かし、今後もグローバルの開発、製造、販売経路を有する大手製薬企業とライセンス契約を締結することで、新たな標的抗原の開発も含め、より大きな市場シェアと収益を狙っていきます。
「共同パイプライン」については、既に複数の国内外の大手製薬企業と提携を行っておりますが、これらの経験を活かし、今後も多数の製薬企業とライセンス契約することで、PRIME技術の第三者による技術評価を確立させるとともに、多数のパイプラインを開発することによるリスクヘッジ及び多様な収益形態の収益機会を得ることによる収益基盤の安定化を図ります。
また、当社による医薬品の研究開発においては、PRIME技術に関するものを中心とした知的財産権やノウハウが重要な経営資源となります。当社は、事業の運営及び拡大に必要な特許権等の知的財産権を、国内外において適時適切に出願及び登録することにより、知的財産権の保護の最大化を図る方針です。当社が出願人である又は当社がライセンスを有する登録済もしくは出願中の特許については、上記「第1 企業の概況 3 事業の内容 (8)知的財産権(特許等)について」をご参照ください。
当社は、その経験とPRIME技術を活かし、固形がんに対する次世代細胞療法を開発すべく、技術、創薬、製造、そして人材の確保と定着に継続的に投資することを通じて、最適な標的抗原の選定を含め、新たな分野である固形がんに対する遺伝子改変免疫細胞療法の研究開発を推し進めることにより、固形がん治療の領域における当社のプレゼンスの向上・確立を図ります。
(3)経営上の目標の達成状況を把握するための客観的な指標等
当社は、現在研究開発段階にあり、売上高、利益率、ROA/ROEその他の数値的な目標となる経営指標等は用いておりません。当社は、「自社創薬」と「共同パイプライン」のハイブリッドビジネスモデルに基づき、PRIME技術の市場への展開や周知を加速化して早期の収益確保を図ると同時に、長期的には大型の販売収益を確保することにより、事業経営におけるリスク分散及びサステナブルな事業成長を実現することを目指し、当社の開発パイプライン及び他社との共同プロジェクトの進捗及びより一層のパイプラインの拡充を目標として事業活動を推進しています。開発中の自社パイプラインについて、非臨床試験の段階においては開発段階を詳細に区切った作業工程表を作成しており、定期的なモニタリングを行い開発の進捗状況を適宜確認し管理しております。第I相臨床試験など臨床試験においては、医療機関での治験実施の患者数等を目標管理しております。
共同パイプラインについては、提携した製薬企業等からの定期的な報告を受け、開発の進捗状況を適宜確認しております。
(4)経営環境
①がん罹患率・生存率について
日本国内において、がんの死亡数と罹患数は、人口の高齢化を主な要因としてともに増加し続けております。男女ともがんの死亡数は増加し続けており、2021年のがん死亡数は、38万人以上と報告されております(出典:国立がん研究センターがん情報サービス「がん統計」(厚生労働省人口動態統計))。同様に、男女ともにがんの罹患数は1985年以降増加し続けており、2019年のがん罹患数は99万人以上と報告されております(国立がん研究センターがん情報サービス「がん統計」(全国がん登録))。また、日本人が生涯でがんに罹患する確率は、男性で65%、女性で51%と報告されており、(出典:国立がん研究センターがん情報サービス「がん統計」(累積罹患リスク(グラフデータベース)))、世界の2020年がん罹患者数は約1,930万人(出典:GLOBOCAN 2020)とされております。また、各がん腫の5年生存率は、特にステージの進んだがんにおいて依然として低く、有効な治療法の開発が急務であります。
 ②遺伝子改変免疫細胞療法の市場について
②遺伝子改変免疫細胞療法の市場についてがんによる死亡数は、2020年において世界で約996万人とされております(WHO CANCER Tomorrow)。世界におけるがん治療薬の市場規模は拡大傾向にあり、2018年にはがん免疫療法の研究開発に対してノーベル生理学・医学賞が授与されたこともあり、がん免疫療法に対する期待が大いに高まっております。さらに、最先端のがん免疫療法として遺伝子改変免疫細胞療法が製薬業界で存在感を高めており、CAR-T細胞を代表とする遺伝子改変T細胞療法の世界市場は2030年において260億ドルに達するとも予測されております(国立研究開発法人科学技術振興機構 戦略プロポーザル「デザイナー細胞」)。

③薬価の動向について
CAR-T細胞療法は、固形がんに対する治療法として上市されたものは現時点では存在しないものの、再発又は難治性のB細胞性急性リンパ芽球性白血病やびまん性大細胞型B細胞リンパ腫といった血液がんに対する治療法として実用化されており、スイスの大手製薬企業のノバルティスファーマが開発したキムリア(一般名:チサゲンレクルユーセル)は、高い完全寛解率(※1)と比較的長期の寛解維持(※2)が臨床試験で実証され、医薬品として2017年8月に米国承認、2018年8月に欧州承認、2019年3月に日本承認となりました。米国での薬価は475,000ドル(約5,200万円)、日本での薬価は3,349万円(収載時の薬価。その後の改定により2021年7月時点では3,264万円)と決定されました。また、日本においては、イエスカルタ(一般名:アキシカブタゲン シロルユーセル)とブレンヤンジ(一般名:リソカブタゲン マラルユーセル)が再発又は難治性の大細胞型B細胞リンパ腫に対して承認されており、アベクマ(一般名:イデカブタゲン ビクルユーセル)が再発又は難治性の多発性骨髄腫に対して承認されています。薬価はキムリアと同額となっております。
※1 完全寛解率:全てのがん病変が消失した患者の割合
※2 寛解維持:全てのがん病変が消失し、再発が確認されていない状態
④希少疾病用品目・先駆的品目の指定制度や早期承認制度等について
厚生労働省が2015年度より試行的に実施していた先駆け審査指定制度は、薬機法において先駆的品目の指定制度として法制化され、2020年9月より施行されております。これは、一定の要件を満たす画期的な医薬品等について、開発の比較的早期の段階から先駆的品目指定制度の対象品目に指定し、薬事承認に関する相談・審査における優先的な取扱いをするものです。加えて、薬機法においては、対象となる患者数が少ないために開発のインセンティブが小さい医薬品等について、一定の要件を満たす場合に、希少疾病用品目としての指定を受けることができるとされております。希少疾病用品目として指定を受けた場合には、優先審査の対象となるほか、助成金の交付や税制上の優遇措置等を受けることができ、これにより、希少疾病に関する医薬品等の開発にインセンティブを付与し、そのアンメットメディカルニーズを解消することが企図されています。当社で現在開発中のCAR-T製剤は、これらの指定制度の対象となりうる品目であることから、当社は研究開発を迅速化させるため、これらの指定制度(海外における同様の制度を含みます。)を活用する可能性があります。
また、当社で現在開発中のCAR-T製剤は、薬機法上の再生医療等製品に該当するものであり、その性質上、製品の有効性を確認するための臨床データの収集、評価に長期間を要する場合があります。他方で、再生医療等製品には条件及び期限付承認制度が存在し、限られた数の症例から有効性が推定でき、安全性が確認された場合には、その適正な使用の確保のために必要な条件及び7年を超えない範囲内の期限付きの承認を得られる可能性があります。
⑤CAR-T細胞療法のグローバルでの開発競争の現状
革新的ながん治療法であるCAR-TやTCR-Tといった遺伝子改変免疫細胞療法はグローバルで開発競争が過熱しており、大手製薬メーカーでは自社での内部開発から他社との共同開発、又は買収による研究開発のスピードアップ戦略に切り替える事例も出始めております。海外のCAR-T研究開発を行うベンチャー企業の大型の買収事例も増えており、2017年8月に米ギリアド・サイエンシズがカイトファーマを約119億ドル(約1兆5,289億円)で買収、2018年1月には米セルジーンがジュノ・セラピューティクスを約90億ドル(約1兆1,563億円)で買収しました。また、近年では特に固形がんの治療を対象に、新たな技術を用いたCAR-T細胞療法の開発を実施するベンチャー企業が国内外で精力的に研究開発を実施しております。中でも当社のPRIME技術はCAR-T細胞を強化するだけでなく体内の免疫も誘導するユニークな技術であります。
(5)優先的に対処すべき事業上及び財務上の課題
当社は、固形がんに対する遺伝子改変免疫細胞療法の研究開発を推進すべく、以下の取組みを進めております。
①PRIME技術の基礎研究体制の拡大及び国内外の学術機関、民間機関等との共同研究開発の推進
当社は、山口大学との共同研究等に基づくPRIME技術の活用により、これまで複数のパイプラインを構築しております。また、中核技術であるPRIME技術の改良や応用についての基礎研究を進めております。今後も山口大学との緊密な連携や国内外の学術機関、民間機関等との共同研究開発により、より一層のパイプラインの拡充、及びPRIME技術の周辺知財の構築を図る方針であり、研究体制の拡充を図って参ります。
②臨床試験の推進
当社は、複数のパイプラインを構築しております。そのうち自社創薬のパイプラインであるNIB101について現在第Ⅰ相臨床試験を実施中であり、当該パイプラインの臨床試験を自社主導で推進し、臨床試験より得られたデータを評価することで、ライセンス先における開発の加速にも資するものと考えております。自社パイプラインで最も進捗しているNIB101については、今後も臨床試験を着実に実施して参ります。
③ライセンス先に対する支援
PRIME技術のライセンス契約を締結した製薬企業に対し、臨床開発が滞りなく進められるよう、当社が技術的アドバイスを行い、また、契約によっては分担業務を行い、ライセンス先との協力を継続的に行っていく方針であります。
④ライセンス契約の拡大に向けた体制拡充
安定した事業ポートフォリオの構築とさらなる収益機会の獲得を目指すため、また「共同パイプライン」におけるライセンス契約をより多くの国内外の製薬企業に広めるため、事業開発人材等の適切な人材の拡充が重要であり、外部人材の確保や人材登用等による人材育成及び活用を図って参ります。
⑤新しい事業機会を得るための外部機関との新たな連携
当社は、パイプライン拡充とともに、新たな形態のパイプラインの構築や、細胞医薬製造の効率化を目指しております。そのため、新たなゲノム編集技術や、遺伝子導入法、自動培養装置などの技術を持つ外部機関との連携の拡大を図っております。
⑥財務基盤の強化
当社はこれまで数度にわたるエクイティファイナンスやパートナー企業からのライセンスに関する収入により資金を調達してまいりましたが、今後さらなる研究開発の推進のため、必要に応じて適切な時期に資金調達を実施し、財務的基盤の強化を図ります。
⑦当社の正社員の採用、育成、登用
当社の主要な業務は、原則として正社員によって運用することを基本方針としております。その理由は、当社の経営理念に深く共感する当社のチームメンバーが、主体性をもって研究開発を行うこと、また、ライセンス先の製薬企業と接することが、事業推進の品質とスピードを向上させ、競合他社に対して大きな差別化の要素となり、当業界における最も優れた競争優位性であると考えているためです。
当社への入社志望者については、それまでの経歴や能力、潜在性を評価・選考し、最終面接時に当社の経営理念の説明を行い、候補者にとって共感できているかどうかを、当社の採用基準としております。採用後の育成については、現場での上長によるOJT(オン・ザ・ジョブ・トレーニング)や、部門長によって個人別に計画した教育研修スケジュールを実施しております。
社内登用については、事前に策定した個人別の目標管理シートに基づいて一定の成果をあげているかどうかを確認し、さらに重ねて当社の経営理念に沿った日常的な行動規範をしているかどうかについて、人事評価委員会による評価会議を経て、部門配置や昇格・昇給及び降格・降給を決定しております。
今後も上記の方法に基づき、研究開発の加速パイプラインの進捗等に対応し、必要に応じて適切かつ十分な人材確保に努めてまいります。