四半期報告書-第23期第1四半期(令和3年1月1日-令和3年3月31日)
(1) 経営成績の分析
当社グループ(当社及び連結子会社3社)は当第1四半期連結累計期間において、新型コロナウイルス感染症に対する予防用ワクチンと治療薬の二軸で国内外で開発を進めてまいりました。HGF遺伝子治療用製品「コラテジェン®」は適用拡大及び米国での承認を目指して、国内外で臨床試験を進めております。また新規ゲノム編集技術を有するEmendoBio Inc.(以下Emendo社といいます。)を完全子会社化し、戦略的提携先との共同開発を進めて開発パイプラインの拡充を図り、遺伝子医薬のグローバルリーダーを目指した事業を推進してまいりました。
2020年12月に子会社化したEmendo社の業績は当第1四半期連結累計期間より連結損益計算書に含めております。
当第1四半期連結累計期間の事業収益は11百万円(前年同期比5百万円(+101.4%)の増収)となりました。当社グループでは、HGF遺伝子治療用製品「コラテジェン®筋注用4mg(以下「コラテジェン®」といいます。)」の販売収入につきまして、製品売上高に計上しております。また、提携企業からの契約一時金、マイルストーンを、研究開発事業収益に計上しております。
当第1四半期連結累計期間において、製品売上高は11万円(前年同期比5百万円(+101.4)の増収)を計上いたしました。研究開発事業収益の計上はありませんでした。
当第1四半期連結累計期間における事業費用は、36億39百万円(前年同期比26億59百万円(+271.5%)の増加)となりました。売上原価は、6百万円(前年同期比3百万円(+100.0%)の増加)となりました。
研究開発費は24億16百万円(前年同期比17億87百万円(+284.5%)の増加)となりました。当第1四半期連結累計期間において、主に新型コロナウイルス感染症予防DNAワクチンの原材料を臨床及び非臨床試験へ使用したことにより、研究用材料費が5億75百万円増加しております。新型コロナウイルス感染症予防DNAワクチンの臨床試験及び非臨床試験の進展により、外注費が7億48百万円増加しております。新型コロナウイルス感染症予防DNAワクチンの研究用試薬・消耗品の購入及び衛生検査所開設に伴う測定機器・試薬等の購入により、消耗品費が2億55百万円増加しております。主にEmendo社を新規連結したことにより、給料手当が1億3百万円増加しております。当社グループのような研究開発型バイオベンチャー企業は先行投資が続きますが、提携戦略などにより財務リスクの低減を図りながら、今後も研究開発投資を行っていく予定です。研究開発の詳細については、本報告書「(4)研究開発活動」をご参照ください。
当第1四半期連結累計期間における販売費及び一般管理費は12億16百万円(前年同期比8億68百万円(+249.5%)の増加)となりました。前年同期と比較して、主に弁護士等専門家への報酬の増額、コンサルタント費用の増加、銀行手数料の増加等により、支払手数料が1億70百万円増加しております。のれん償却額が発生したことに伴い、減価償却費が5億67百万円増加しております。
この結果、当第1四半期連結累計期間の営業損失は36億28百万円(前年同期の営業損失は9億74百万円)となり、前年同期より26億54百万円損失が拡大しております。
当第1四半期連結累計期間の経常損失は、33億61百万円(前年同期の経常損失は9億22百万円)となりました。外貨預金及びEmendo社への貸付金の評価替に伴い、為替差益が2億81百万円発生しております。新株予約権の発行及び行使に伴う株式交付費が33百万円発生し、前年同期に比べ11百万円増加しております。
当第1四半期連結累計期間の親会社株主に帰属する四半期純損失は、33億14百万円(前年同期の親会社株主に帰属する四半期純損失は9億19百万円)となりました。ストック・オプションの権利行使期間終了による権利失効に伴い、新株予約権戻入益が32百万円発生しております。
(2) 財政状態の分析
当第1四半期連結会計期間末の総資産は422億61百万円(前連結会計年度末比39億7百万円の増加)となりました。新株予約権の発行及び行使に伴う58億45百万円の入金はありましたが、当期事業費用への充当により、現金及び預金は26億20百万円増加し、141億57百万円となりました。新型コロナウイルス感染症予防DNAワクチンの製造費用を前払いしたことに伴い、前渡金が3億53百万円増加して14億14百万円となりました。未収消費税等が1億74百万円増加して4億55百万円となりました。流動資産は31億51百万円増加し、173億18百万円となっております。
固定資産においては、のれんの償却による5億67百万円の減少及び為替換算による14億3百万円の増加により、のれんが8億35百万円増加して235億49百万円となり、固定資産は7億55百万円増加し、249億43百万円となっております。
当第1四半期連結会計期間末の負債は56億97百万円(前連結会計年度末比22百万円の増加)となりました。主に新型コロナウイルス感染症予防DNAワクチンの製造に係る費用及び治験費用等の計上により、買掛金が2億80百万円増加しております。前年度の費用の支払により、未払金が8億96百万円減少しております。国立研究開発法人日本医療研究開発機構(AMED)より採択された「新型コロナウイルス感染症(COVID-19)に対するワクチン開発」に関する助成金が入金され、前受金が6億93百万円増加しております。前年度の法人事業税等の支払により、未払法人税等が85百万円減少しております。
純資産は365億64百万円(前連結会計年度末比38億84百万円の増加)となりました。新株予約権の発行及び行使により、資本金及び資本剰余金がそれぞれ29億円増加し、新株予約権が11百万円増加しております。親会社株主に帰属する四半期純損失33億14百万円の計上により、利益剰余金が減少しております。在外子会社に係る為替換算により、為替換算調整勘定が13億94百万円増加しております。
(3) 事業上及び財務上の対処すべき課題
当第1四半期連結累計期間において、当社グループの事業上及び財務上の対処すべき課題に重要な変更、及び新たに生じた課題はありません。
(4) 研究開発活動
当第1四半期連結累計期間における研究開発費は24億16百万円(前年同期比17億87百万円(+284.5%)の増加)となりました。
当社グループは、“遺伝子医薬のグローバルリーダー”を目指し、遺伝子治療を中心に医薬品開発に取り組んでおります。中でも2019年末から拡大している新型コロナウイルス感染症に関しては、予防用のワクチンと治療薬の二軸で、国内外で開発を進めております。また、究極の遺伝子治療であるゲノム編集においては、先進の技術を持つEmendo社を完全子会社とし、共にゲノム編集技術で、いままで治療法のなかった患者にお届けできる医薬品開発を進めてまいります。 2019年9月に製品化したHGF遺伝子治療用製品「コラテジェン®」は、適応拡大及び米国での承認を目指して、国内外で臨床試験を実施しております。導出に向けた活動も積極的に行い、トルコのEr-Kim社と独占販売契約を締結いたしました。椎間板性腰痛症を対象としてNF-κBデコイオリゴDNAや高血圧向けDNAワクチンの開発も継続して行っております。当社は、海外企業との提携も積極的に行い、有望な医薬品の実用化に向けて共同開発を進めております。
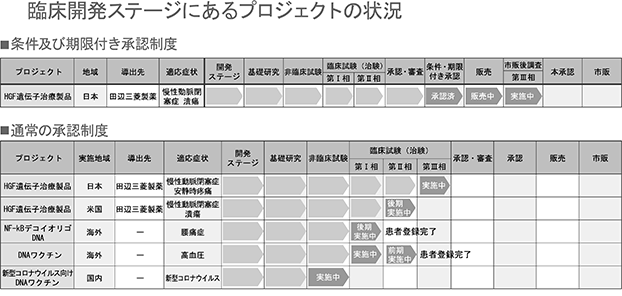
■新型コロナウイルス感染症予防DNAワクチン(自社品)
当社は、プラスミドDNAの技術を用いて2020年3月より大阪大学と共同で新型コロナウイルス感染症に対する予防用ワクチンの開発を開始し、現在実施中の第Ⅱ/Ⅲ相臨床試験において、2021年3月に500症例の接種を完了しました。
■新型コロナウイルス感染症治療薬(共同開発品)
当社は、カナダのバイオ医薬品企業であるVasomune社と急性呼吸不全など血管の不全を原因とする疾患を対象とした医薬品に関する共同開発契約を締結しました。現在AV-001を新型コロナウイルス感染症治療薬として、2020年12月より健康成人を対象とした第Ⅰ相臨床試験を米国において実施し、安全性と忍容性を認め、良好な結果を確認しました。続く第Ⅱ相臨床試験では、米国とカナダの2か国での実施として準備を進めております。
■HGF遺伝子治療用製品(一般名:ベペルミノゲンペルプラスミド)(自社品)
⦅対象疾患:慢性動脈閉塞症⦆
慢性動脈閉塞症を対象疾患としたHGF遺伝子治療用製品の開発については、「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(医薬品医療機器等法)」により再生医療等製品の早期実用化を目的とした「条件及び期限付承認制度」(2014年11月施行)を活用し、2019年3月に国内初の遺伝子治療用製品「コラテジェン®」として、慢性動脈閉塞症の潰瘍の改善効能効果で条件及び期限付承認を取得し、2019年9月10日より発売を開始いたしました。
田辺三菱製薬株式会社(以下「田辺三菱製薬」といいます。)と当社は、HGF遺伝子治療用製品「コラテジェン®」の販売に関し、日本及び米国における末梢性血管疾患を対象とした独占的販売権許諾契約を締結しており、田辺三菱製薬が販売を担当いたしております。今回の承認は、条件及び期限付であり、製造販売後承認条件評価を2024年までに行い、本承認取得を目指してまいります。海外開発については、米国において2020年1月より、下肢潰瘍を有する閉塞性動脈硬化症を対象とした第Ⅱb相臨床試験を実施しております。
⦅対象疾患:慢性動脈閉塞症における安静時疼痛⦆
「コラテジェン®」の適応拡大を目的として、国内において慢性動脈閉塞症における安静時疼痛を有する患者を対象にした第Ⅲ相臨床試験を2019年10月より実施しております。
■NF-κBデコイオリゴDNA
⦅対象疾患:椎間板性腰痛症(自社品)⦆
核酸医薬NF-κBデコイオリゴDNAについては椎間板性腰痛症を含む腰痛疾患を適応症とした開発を進めております。2018年2月より椎間板性腰痛症を対象とした第Ⅰb相臨床試験は、投与後の観察期間6カ月間に続き、12ケ月間を経た結果でも、患者の忍容性は高いうえ、重篤な有害事象も認められず、安全性を確認できました。さらに、探索的にデータを評価したところ、患者の腰痛に著しい軽減とその効果の持続が認められ、有効性も確認できました。今後引き続きデータ分析を行い、第Ⅱ相臨床試験へ移行することとなります。
核酸医薬デコイオリゴDNAのその他の開発については、これまでNF-κBデコイオリゴDNAの次世代型デコイオリゴDNAとして、炎症に関わるNF-κBとSTAT6という2つの重要な転写因子を同時に抑制する働きを持った「キメラデコイ」の開発を進めております。NF-κBのみをターゲットとした従来のデコイオリゴDNAと比較して、より強力で幅広い炎症抑制効果を発揮することが期待されます。
■高血圧治療用DNAワクチン(自社品)
当社グループは、遺伝子治療用製品、核酸医薬につづく遺伝子医薬の第三の事業として、DNAワクチンの開発を手がけており、高血圧治療用DNAワクチンの開発を進めております。オーストラリアでの第Ⅰ/Ⅱa相臨床試験は投与後の初期の試験結果の評価を行ったところ、重篤な有害事象はなく、安全性に問題がないことを確認し、アンジオテンシンⅡに対する抗体産生を認めました。今後、安全性、免疫原性および有効性を評価する試験を継続的に行ってまいります。
新規研究開発プロジェクト及び新規事業プロジェクト
■ゲノム編集技術による遺伝子治療用製品開発
当社は、究極の遺伝子治療法ともいわれるゲノム編集技術を用いた遺伝子疾患治療に挑むため、2020年12月にゲノム編集における先進技術及びそれを活用した開発パイプラインを持つEmendo社へ追加出資し、完全子会社化しました。Emendo社のゲノム編集技術は、高い効率で正確なゲノム編集を可能にする画期的かつ実用的な独自技術です。
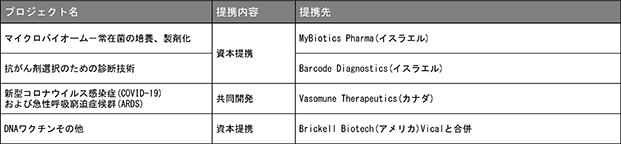
■マイクロバイオームを用いた疾患予防・健康維持
当社は、腸内細菌叢を利用した疾患治癒の薬品や健康維持のサプリメントについて開発しているイスラエルのMyBiotics Pharma Ltd.と2018年7月に資本提携し、1 人 1 人の健康状態・体質に合った腸内細菌を見つけ出し、それらを含む薬品やサプリメントを開発することを目指しています。
■抗がん剤診断事業への参入
当社は、事業基盤拡大を目的としイスラエルのバイオハイテク企業Barcode Diagnostics Ltd.が開発した、個々のがん患者にとって最適な抗がん剤を迅速に特定する診断技術の早期実用化に向け、2020年2月に公益財団法人がん研究会と共同研究契約を締結いたしました。
■Brickell Biotech,Inc.(旧:バイカル社)との戦略的な開発協力
当社と2016年12月に戦略的事業提携を締結したバイカル社は、2019年8月に米国のBrickell Biotech, Inc.との合併契約を締結し、合併後の新社名はBrickell Biotech, Inc.となりました。同社とは2020年9月に新型コロナウイルス感染症予防DNAワクチンの米国での臨床開発に関する共同開発契約を締結しました。
(5) 事業のリスクに記載した重要事象等についての分析及び改善するための対応方法
医薬品事業は、製品化までに多額の資金と長い時間を要する等の特性があり、創薬ベンチャーである当社グループにおいては、継続的な営業損失の発生及び営業キャッシュ・フローのマイナスを計上している状況にあります。そのため、継続企業の前提に重要な疑義を生じさせるような状況が存在しております。
当社グループは当該状況を解消すべく、下記を重要な課題として取り組んでおります。
①自社既存プロジェクトの推進
当社グループでは、2019年3月に国内初の遺伝子治療用製品「コラテジェン®」の条件及び期限付承認を厚生労働省から取得し、同年9月から販売を開始いたしました。現在、製造販売後承認条件評価を行うとともに国内での同製品の適用拡大のための臨床試験及び米国での閉塞性動脈硬化症を対象とした臨床試験を進めております。また、現在海外で臨床試験を進めております椎間板性腰痛症向けの核酸医薬NF-κBデコイオリゴDNA、高血圧DNAワクチンを含めた3プロジェクトを推進しております。これらのプロジェクトを確実に推進していくことが最優先課題であると考えております。
②開発パイプラインの拡充と事業基盤の拡大
当社グループでは新型コロナウイルス感染症の世界的な蔓延を機に予防用としてのDNAワクチンの開発を2020年3月より開始し、現在第Ⅱ/Ⅲ相の臨床試験を実施しております。また、ゲノム編集における先進技術を持つEmendo社を完全子会社化し、究極の遺伝子治療ともいわれるゲノム編集で世界に戦いを挑みます。これらの開発パイプラインの拡充や事業基盤の拡大により、当社グループは遺伝子治療の世界でグローバルリーダーを目指します。
今後も、ライセンス導入や共同開発、創薬プラットフォーム技術の獲得を目指した事業提携に加え、他社に対する資本参加や他社の買収等により開発品パイプラインの拡充による事業基盤の拡大を図り、将来の成長を実現してまいります。
③開発プロジェクトにおける提携先の確保
当社グループでは、開発プロジェクトのリスクを低減するために、製薬会社と提携し、契約金・マイルストーンや開発協力金を受け取ることにより財務リスクを低減しながら開発を進めるという提携モデルを基本方針としております。
「コラテジェン®」について日本と米国を対象とした独占的販売契約を田辺三菱製薬と締結しており、マイルストーン収入やロイヤリティー収入が見込めます。また、2019年2月にイスラエルにおけるHGF遺伝子治療用製品「コラテジェン®」の独占的販売権の許諾について同国Kamada社と基本合意書を締結しております。さらに2020年10月にスペシャルティ薬(特定疾患専門薬)を扱うトルコのEr-Kim社と「コラテジェン®」のトルコでの導出(独占的販売権許諾)に関する基本合意書を締結しました。椎間板性腰痛症向けの核酸医薬NF-κBデコイオリゴDNA、高血圧DNAワクチンにつきましては臨床試験が予定どおり進捗しており、製薬企業等への早期導出により契約一時金、ロイヤリティー等を得ることにより、開発費の負担削減と定期的な収入確保を目指してまいります。今後も、製薬会社との提携を進めることにより、事業基盤の強化に努めてまいります。
④資金調達の実施
当社グループにとって、研究開発活動及び事業基盤の拡大を推進することは継続的な発展のために重要であり、そのためには状況に応じ機動的に資金調達を行うことが必要となります。2021年3月8日開催の取締役会において、第41回新株予約権(第三者割当て)(行使価額修正条項付)の発行を決議し、2021年5月13日までにその一部が行使され160億94百万円(新株予約権発行による入金を含む)を調達いたしました。今後も、研究開発活動推進及び企業維持のために必要となる資金調達の可能性を適宜検討してまいります。
これら諸施策の実施により、継続企業の前提に関する重要な不確実性は認められないと判断しております。
当社グループ(当社及び連結子会社3社)は当第1四半期連結累計期間において、新型コロナウイルス感染症に対する予防用ワクチンと治療薬の二軸で国内外で開発を進めてまいりました。HGF遺伝子治療用製品「コラテジェン®」は適用拡大及び米国での承認を目指して、国内外で臨床試験を進めております。また新規ゲノム編集技術を有するEmendoBio Inc.(以下Emendo社といいます。)を完全子会社化し、戦略的提携先との共同開発を進めて開発パイプラインの拡充を図り、遺伝子医薬のグローバルリーダーを目指した事業を推進してまいりました。
2020年12月に子会社化したEmendo社の業績は当第1四半期連結累計期間より連結損益計算書に含めております。
当第1四半期連結累計期間の事業収益は11百万円(前年同期比5百万円(+101.4%)の増収)となりました。当社グループでは、HGF遺伝子治療用製品「コラテジェン®筋注用4mg(以下「コラテジェン®」といいます。)」の販売収入につきまして、製品売上高に計上しております。また、提携企業からの契約一時金、マイルストーンを、研究開発事業収益に計上しております。
当第1四半期連結累計期間において、製品売上高は11万円(前年同期比5百万円(+101.4)の増収)を計上いたしました。研究開発事業収益の計上はありませんでした。
当第1四半期連結累計期間における事業費用は、36億39百万円(前年同期比26億59百万円(+271.5%)の増加)となりました。売上原価は、6百万円(前年同期比3百万円(+100.0%)の増加)となりました。
研究開発費は24億16百万円(前年同期比17億87百万円(+284.5%)の増加)となりました。当第1四半期連結累計期間において、主に新型コロナウイルス感染症予防DNAワクチンの原材料を臨床及び非臨床試験へ使用したことにより、研究用材料費が5億75百万円増加しております。新型コロナウイルス感染症予防DNAワクチンの臨床試験及び非臨床試験の進展により、外注費が7億48百万円増加しております。新型コロナウイルス感染症予防DNAワクチンの研究用試薬・消耗品の購入及び衛生検査所開設に伴う測定機器・試薬等の購入により、消耗品費が2億55百万円増加しております。主にEmendo社を新規連結したことにより、給料手当が1億3百万円増加しております。当社グループのような研究開発型バイオベンチャー企業は先行投資が続きますが、提携戦略などにより財務リスクの低減を図りながら、今後も研究開発投資を行っていく予定です。研究開発の詳細については、本報告書「(4)研究開発活動」をご参照ください。
当第1四半期連結累計期間における販売費及び一般管理費は12億16百万円(前年同期比8億68百万円(+249.5%)の増加)となりました。前年同期と比較して、主に弁護士等専門家への報酬の増額、コンサルタント費用の増加、銀行手数料の増加等により、支払手数料が1億70百万円増加しております。のれん償却額が発生したことに伴い、減価償却費が5億67百万円増加しております。
この結果、当第1四半期連結累計期間の営業損失は36億28百万円(前年同期の営業損失は9億74百万円)となり、前年同期より26億54百万円損失が拡大しております。
当第1四半期連結累計期間の経常損失は、33億61百万円(前年同期の経常損失は9億22百万円)となりました。外貨預金及びEmendo社への貸付金の評価替に伴い、為替差益が2億81百万円発生しております。新株予約権の発行及び行使に伴う株式交付費が33百万円発生し、前年同期に比べ11百万円増加しております。
当第1四半期連結累計期間の親会社株主に帰属する四半期純損失は、33億14百万円(前年同期の親会社株主に帰属する四半期純損失は9億19百万円)となりました。ストック・オプションの権利行使期間終了による権利失効に伴い、新株予約権戻入益が32百万円発生しております。
(2) 財政状態の分析
当第1四半期連結会計期間末の総資産は422億61百万円(前連結会計年度末比39億7百万円の増加)となりました。新株予約権の発行及び行使に伴う58億45百万円の入金はありましたが、当期事業費用への充当により、現金及び預金は26億20百万円増加し、141億57百万円となりました。新型コロナウイルス感染症予防DNAワクチンの製造費用を前払いしたことに伴い、前渡金が3億53百万円増加して14億14百万円となりました。未収消費税等が1億74百万円増加して4億55百万円となりました。流動資産は31億51百万円増加し、173億18百万円となっております。
固定資産においては、のれんの償却による5億67百万円の減少及び為替換算による14億3百万円の増加により、のれんが8億35百万円増加して235億49百万円となり、固定資産は7億55百万円増加し、249億43百万円となっております。
当第1四半期連結会計期間末の負債は56億97百万円(前連結会計年度末比22百万円の増加)となりました。主に新型コロナウイルス感染症予防DNAワクチンの製造に係る費用及び治験費用等の計上により、買掛金が2億80百万円増加しております。前年度の費用の支払により、未払金が8億96百万円減少しております。国立研究開発法人日本医療研究開発機構(AMED)より採択された「新型コロナウイルス感染症(COVID-19)に対するワクチン開発」に関する助成金が入金され、前受金が6億93百万円増加しております。前年度の法人事業税等の支払により、未払法人税等が85百万円減少しております。
純資産は365億64百万円(前連結会計年度末比38億84百万円の増加)となりました。新株予約権の発行及び行使により、資本金及び資本剰余金がそれぞれ29億円増加し、新株予約権が11百万円増加しております。親会社株主に帰属する四半期純損失33億14百万円の計上により、利益剰余金が減少しております。在外子会社に係る為替換算により、為替換算調整勘定が13億94百万円増加しております。
(3) 事業上及び財務上の対処すべき課題
当第1四半期連結累計期間において、当社グループの事業上及び財務上の対処すべき課題に重要な変更、及び新たに生じた課題はありません。
(4) 研究開発活動
当第1四半期連結累計期間における研究開発費は24億16百万円(前年同期比17億87百万円(+284.5%)の増加)となりました。
当社グループは、“遺伝子医薬のグローバルリーダー”を目指し、遺伝子治療を中心に医薬品開発に取り組んでおります。中でも2019年末から拡大している新型コロナウイルス感染症に関しては、予防用のワクチンと治療薬の二軸で、国内外で開発を進めております。また、究極の遺伝子治療であるゲノム編集においては、先進の技術を持つEmendo社を完全子会社とし、共にゲノム編集技術で、いままで治療法のなかった患者にお届けできる医薬品開発を進めてまいります。 2019年9月に製品化したHGF遺伝子治療用製品「コラテジェン®」は、適応拡大及び米国での承認を目指して、国内外で臨床試験を実施しております。導出に向けた活動も積極的に行い、トルコのEr-Kim社と独占販売契約を締結いたしました。椎間板性腰痛症を対象としてNF-κBデコイオリゴDNAや高血圧向けDNAワクチンの開発も継続して行っております。当社は、海外企業との提携も積極的に行い、有望な医薬品の実用化に向けて共同開発を進めております。

■新型コロナウイルス感染症予防DNAワクチン(自社品)
当社は、プラスミドDNAの技術を用いて2020年3月より大阪大学と共同で新型コロナウイルス感染症に対する予防用ワクチンの開発を開始し、現在実施中の第Ⅱ/Ⅲ相臨床試験において、2021年3月に500症例の接種を完了しました。
■新型コロナウイルス感染症治療薬(共同開発品)
当社は、カナダのバイオ医薬品企業であるVasomune社と急性呼吸不全など血管の不全を原因とする疾患を対象とした医薬品に関する共同開発契約を締結しました。現在AV-001を新型コロナウイルス感染症治療薬として、2020年12月より健康成人を対象とした第Ⅰ相臨床試験を米国において実施し、安全性と忍容性を認め、良好な結果を確認しました。続く第Ⅱ相臨床試験では、米国とカナダの2か国での実施として準備を進めております。
■HGF遺伝子治療用製品(一般名:ベペルミノゲンペルプラスミド)(自社品)
⦅対象疾患:慢性動脈閉塞症⦆
慢性動脈閉塞症を対象疾患としたHGF遺伝子治療用製品の開発については、「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(医薬品医療機器等法)」により再生医療等製品の早期実用化を目的とした「条件及び期限付承認制度」(2014年11月施行)を活用し、2019年3月に国内初の遺伝子治療用製品「コラテジェン®」として、慢性動脈閉塞症の潰瘍の改善効能効果で条件及び期限付承認を取得し、2019年9月10日より発売を開始いたしました。
田辺三菱製薬株式会社(以下「田辺三菱製薬」といいます。)と当社は、HGF遺伝子治療用製品「コラテジェン®」の販売に関し、日本及び米国における末梢性血管疾患を対象とした独占的販売権許諾契約を締結しており、田辺三菱製薬が販売を担当いたしております。今回の承認は、条件及び期限付であり、製造販売後承認条件評価を2024年までに行い、本承認取得を目指してまいります。海外開発については、米国において2020年1月より、下肢潰瘍を有する閉塞性動脈硬化症を対象とした第Ⅱb相臨床試験を実施しております。
⦅対象疾患:慢性動脈閉塞症における安静時疼痛⦆
「コラテジェン®」の適応拡大を目的として、国内において慢性動脈閉塞症における安静時疼痛を有する患者を対象にした第Ⅲ相臨床試験を2019年10月より実施しております。
■NF-κBデコイオリゴDNA
⦅対象疾患:椎間板性腰痛症(自社品)⦆
核酸医薬NF-κBデコイオリゴDNAについては椎間板性腰痛症を含む腰痛疾患を適応症とした開発を進めております。2018年2月より椎間板性腰痛症を対象とした第Ⅰb相臨床試験は、投与後の観察期間6カ月間に続き、12ケ月間を経た結果でも、患者の忍容性は高いうえ、重篤な有害事象も認められず、安全性を確認できました。さらに、探索的にデータを評価したところ、患者の腰痛に著しい軽減とその効果の持続が認められ、有効性も確認できました。今後引き続きデータ分析を行い、第Ⅱ相臨床試験へ移行することとなります。
核酸医薬デコイオリゴDNAのその他の開発については、これまでNF-κBデコイオリゴDNAの次世代型デコイオリゴDNAとして、炎症に関わるNF-κBとSTAT6という2つの重要な転写因子を同時に抑制する働きを持った「キメラデコイ」の開発を進めております。NF-κBのみをターゲットとした従来のデコイオリゴDNAと比較して、より強力で幅広い炎症抑制効果を発揮することが期待されます。
■高血圧治療用DNAワクチン(自社品)
当社グループは、遺伝子治療用製品、核酸医薬につづく遺伝子医薬の第三の事業として、DNAワクチンの開発を手がけており、高血圧治療用DNAワクチンの開発を進めております。オーストラリアでの第Ⅰ/Ⅱa相臨床試験は投与後の初期の試験結果の評価を行ったところ、重篤な有害事象はなく、安全性に問題がないことを確認し、アンジオテンシンⅡに対する抗体産生を認めました。今後、安全性、免疫原性および有効性を評価する試験を継続的に行ってまいります。
新規研究開発プロジェクト及び新規事業プロジェクト
■ゲノム編集技術による遺伝子治療用製品開発
当社は、究極の遺伝子治療法ともいわれるゲノム編集技術を用いた遺伝子疾患治療に挑むため、2020年12月にゲノム編集における先進技術及びそれを活用した開発パイプラインを持つEmendo社へ追加出資し、完全子会社化しました。Emendo社のゲノム編集技術は、高い効率で正確なゲノム編集を可能にする画期的かつ実用的な独自技術です。
■マイクロバイオームを用いた疾患予防・健康維持
当社は、腸内細菌叢を利用した疾患治癒の薬品や健康維持のサプリメントについて開発しているイスラエルのMyBiotics Pharma Ltd.と2018年7月に資本提携し、1 人 1 人の健康状態・体質に合った腸内細菌を見つけ出し、それらを含む薬品やサプリメントを開発することを目指しています。
■抗がん剤診断事業への参入
当社は、事業基盤拡大を目的としイスラエルのバイオハイテク企業Barcode Diagnostics Ltd.が開発した、個々のがん患者にとって最適な抗がん剤を迅速に特定する診断技術の早期実用化に向け、2020年2月に公益財団法人がん研究会と共同研究契約を締結いたしました。
■Brickell Biotech,Inc.(旧:バイカル社)との戦略的な開発協力
当社と2016年12月に戦略的事業提携を締結したバイカル社は、2019年8月に米国のBrickell Biotech, Inc.との合併契約を締結し、合併後の新社名はBrickell Biotech, Inc.となりました。同社とは2020年9月に新型コロナウイルス感染症予防DNAワクチンの米国での臨床開発に関する共同開発契約を締結しました。

(5) 事業のリスクに記載した重要事象等についての分析及び改善するための対応方法
医薬品事業は、製品化までに多額の資金と長い時間を要する等の特性があり、創薬ベンチャーである当社グループにおいては、継続的な営業損失の発生及び営業キャッシュ・フローのマイナスを計上している状況にあります。そのため、継続企業の前提に重要な疑義を生じさせるような状況が存在しております。
当社グループは当該状況を解消すべく、下記を重要な課題として取り組んでおります。
①自社既存プロジェクトの推進
当社グループでは、2019年3月に国内初の遺伝子治療用製品「コラテジェン®」の条件及び期限付承認を厚生労働省から取得し、同年9月から販売を開始いたしました。現在、製造販売後承認条件評価を行うとともに国内での同製品の適用拡大のための臨床試験及び米国での閉塞性動脈硬化症を対象とした臨床試験を進めております。また、現在海外で臨床試験を進めております椎間板性腰痛症向けの核酸医薬NF-κBデコイオリゴDNA、高血圧DNAワクチンを含めた3プロジェクトを推進しております。これらのプロジェクトを確実に推進していくことが最優先課題であると考えております。
②開発パイプラインの拡充と事業基盤の拡大
当社グループでは新型コロナウイルス感染症の世界的な蔓延を機に予防用としてのDNAワクチンの開発を2020年3月より開始し、現在第Ⅱ/Ⅲ相の臨床試験を実施しております。また、ゲノム編集における先進技術を持つEmendo社を完全子会社化し、究極の遺伝子治療ともいわれるゲノム編集で世界に戦いを挑みます。これらの開発パイプラインの拡充や事業基盤の拡大により、当社グループは遺伝子治療の世界でグローバルリーダーを目指します。
今後も、ライセンス導入や共同開発、創薬プラットフォーム技術の獲得を目指した事業提携に加え、他社に対する資本参加や他社の買収等により開発品パイプラインの拡充による事業基盤の拡大を図り、将来の成長を実現してまいります。
③開発プロジェクトにおける提携先の確保
当社グループでは、開発プロジェクトのリスクを低減するために、製薬会社と提携し、契約金・マイルストーンや開発協力金を受け取ることにより財務リスクを低減しながら開発を進めるという提携モデルを基本方針としております。
「コラテジェン®」について日本と米国を対象とした独占的販売契約を田辺三菱製薬と締結しており、マイルストーン収入やロイヤリティー収入が見込めます。また、2019年2月にイスラエルにおけるHGF遺伝子治療用製品「コラテジェン®」の独占的販売権の許諾について同国Kamada社と基本合意書を締結しております。さらに2020年10月にスペシャルティ薬(特定疾患専門薬)を扱うトルコのEr-Kim社と「コラテジェン®」のトルコでの導出(独占的販売権許諾)に関する基本合意書を締結しました。椎間板性腰痛症向けの核酸医薬NF-κBデコイオリゴDNA、高血圧DNAワクチンにつきましては臨床試験が予定どおり進捗しており、製薬企業等への早期導出により契約一時金、ロイヤリティー等を得ることにより、開発費の負担削減と定期的な収入確保を目指してまいります。今後も、製薬会社との提携を進めることにより、事業基盤の強化に努めてまいります。
④資金調達の実施
当社グループにとって、研究開発活動及び事業基盤の拡大を推進することは継続的な発展のために重要であり、そのためには状況に応じ機動的に資金調達を行うことが必要となります。2021年3月8日開催の取締役会において、第41回新株予約権(第三者割当て)(行使価額修正条項付)の発行を決議し、2021年5月13日までにその一部が行使され160億94百万円(新株予約権発行による入金を含む)を調達いたしました。今後も、研究開発活動推進及び企業維持のために必要となる資金調達の可能性を適宜検討してまいります。
これら諸施策の実施により、継続企業の前提に関する重要な不確実性は認められないと判断しております。